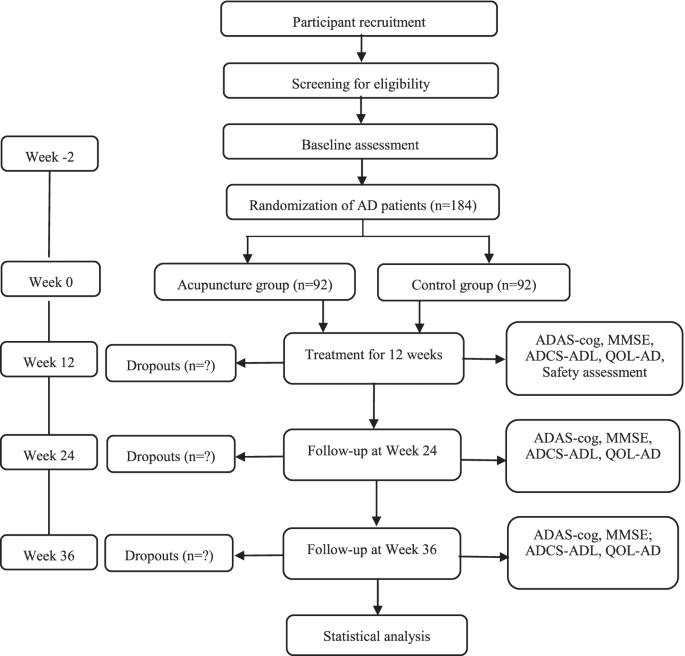
研究背景
该试验将在上海的三家医院(上海中医药大学龙华医院、上海交通大学医学院心理健康中心和复旦大学华山医院)进行。
入选标准
本研究将纳入患者(1)年龄50-85岁;(2)符合美国国家神经和交际障碍与中风研究所(NINCDS)和阿尔茨海默病及相关疾病协会的AD诊断标准的患者[40];(3)使用MMSE(中文版)评估认知障碍,小学和初中教育程度评分为11-22分,高等教育程度评分为11-26分;(4)年龄< 75岁和≥75岁患者的内侧颞叶萎缩评分量表得分分别为≥2和≥3;(5)经本人或监护人签署知情同意书。
排除标准
如果患者的认知功能障碍是由其他疾病引起的(包括血管性痴呆、路易体痴呆、激素或代谢异常、甲状腺功能减退、维生素b12或叶酸缺乏、谵妄或其他情感和精神障碍),则排除在外;(2)患有严重慢性疾病,包括心脏病、肝肾疾病、造血系统疾病;(3)因失语、思维混乱等原因不能配合学习考试的;(4)正在服用抗凝血药物,包括华法林或肝素;(5)前2周内是否接受过针灸治疗。
终止条件
在临床研究过程中,如果受试者出现严重的不良事件或不良反应,在受试者和研究人员讨论过情况并共同同意受试者不能继续进行的情况下,试验将暂停。此外,如果在临床研究过程中,受试者认为他们缺乏疗效,他们将被给予暂停试验的选择。
退出标准
以下脱落标准被用于从研究中撤出患者。(1)研究期间接受过其他AD药物治疗的受试者;(2)未按时到医院随访,且无法通过电话或短信联系的受试者;(3)不愿继续参与研究,并自愿撤回知情同意的受试者。
干预措施
本RCT将招募184例轻中度AD患者,随机分为两组:AG组和CG组。总干事(n= 92)的患者将采用针灸联合盐酸多奈哌齐5毫克/天治疗12周,而CG (n= 92)患者只接受盐酸多奈哌齐5毫克/天,持续12周。两组患者在随访期间均接受常规临床治疗。评价时间点为治疗开始后第12周、24周(随访)、36周(随访)。
针灸治疗
主要穴位为GV 20、GV 24、EX-HN 1、EX-HN 3、GB12、GB39、KI6(穴位位置;见表1).指导医生根据中医辨证论治标准术语参考文献[41].心气虚包括健忘(必需)、表情淡漠、反应迟钝、不善沟通、困倦、声音低沉、易惊(以上3种及以上)、面色苍白、脉搏微弱。肾精虚包括健忘(必需)、懈怠、操作错误、流畅性丧失、头倾背屈、大小便失禁(以上三种或三种以上),脉搏细弱。
心气虚证患者采用HT7、PC6合穴,肾精虚证患者采用KI3、BL23合穴。
患者为仰卧位。消毒后,用一次性不锈钢针(0.25mm×40mm)快速刺穿头皮或皮肤表面,头部呈15°角,四肢和躯干呈90°角。针插入到规定深度后,针会扭曲30秒左右,有酸、麻、沉等德气感。患者将接受治疗每次30分钟,每周三次(每隔一天),持续12周。同时电刺激GV20、GV24穴(2/50 Hz,扩张波)。所有的治疗都将由一位熟练的高级针灸师进行。
每次针灸治疗后,医生都会仔细观察患者是否有疼痛、皮下血肿等不适。治疗结束后,患者将在诊所观察15分钟。
医学治疗
患者将接受盐酸多奈哌齐5毫克,每天治疗12周。在试验期间,参与者将被禁止使用其他治疗AD的药物。根据试验药物的随机编码序列和病例数分配试验药物。每个研究单位将有一个试验药物管理员。研究者将筛选合格的参与者。在知情同意并撰写研究病历后,试验用药管理员将根据患者就诊顺序和药物编码对参与者进行从小到大的分配药物安排;此外,它们将被登记在“临床试验药物使用记录表”中。
后续
所有参与者将接受为期12周的治疗。随后,他们将进入24周的随访期。在第24周和第36周,患者将使用MMSE、阿尔茨海默病合作研究-日常生活活动(ADCS-ADL)量表和阿尔茨海默病生活质量(QOL-AD)量表重新评估。
结果测量
疗效评分由上海市精神卫生中心培训的临床神经学家和精神病学家进行。每次计分由两名记分员分别进行,如果结果不一致,则由第三名记分员作出裁决。所有评分者在评分时都不知道患者的分组。表格2显示了在研究期间使用的干预和评估时间点。
基本特征变量
信息问卷将用于收集年龄、性别、教育背景、婚姻状况、既往病史、病程、MMSE分数等信息。此外,参与者将接受干预前血液检测,以检测淀粉样前体蛋白、载脂蛋白E4和早老素-1,以及磁共振成像(MRI)扫描,以确定诊断。护士将测量并记录病人的生命体征。
主要结果测量
在第12周(干预结束)评估的ADAS-cog是研究的主要结果。量表包含40个项目,用于评估AD患者认知行为障碍的严重程度[42].在本次试验中,我们选择了中文版的ADAS-cog量表,该量表包含12个条目[43,44].该量表的总分从0(无错误或损坏)到75(严重损坏)。得分越高表明认知障碍越严重。一般来说,没有AD或其他痴呆症类型的个体得分为5分。
次要结果测量
ADAS-cog随访
参与者的认知功能也将在第24周(随访)和第36周(随访)使用ADAS-cog量表进行评估。
ADCS-ADL
ADCS-ADL量表主要用于评估痴呆症患者的日常生活活动。目前最常用的ADCS-ADL是由Lawton和Brody于1969年开发的,分为身体自我维护和日常生活量表的工具活动。它包含了19个领域,涉及打电话、购物、做饭、做家务、洗衣、交通、吃药和理财[45].ADCS-ADL总分为54分。得分越高,患者与认知相关的生活质量越好。参与者将在基线、第12周(干预结束)、第24周(随访)和第36周(随访)使用ADCS-ADL进行评估。
患者的
MMSE是1975年设计的,作为痴呆症和精神障碍患者的筛查工具。它由两部分组成:第一部分评估方向、记忆和注意力,而第二部分评估命名能力、口头和书面命令的执行、自发地写句子和复制复杂的多边形。项目的正确性或错误(0,错误;1,正确),结果是正确回答的总数。MMSE得分上限为30分,测试不计时[46].MMSE评分标准与教育程度相关。分数在27到30之间是正常的。MMSE将在基线、第12周(干预结束)、第24周(随访)和第36周(随访)进行测量。
QOL-AD
生活质量-AD量表于1999年开发,用于评估AD患者及其护理人员的生活质量[47].它由13个项目组成,涉及身心健康、生活质量、社会和财务评估。响应选项分为四个级别(1、差;4、优秀的)。分数范围从13到52 [48, 52分代表生活质量最高。将在基线、第12周(干预结束)、第24周(随访)和第36周(随访)测量QOL-AD。
安全
在筛查阶段和治疗后(第12周),参与者将被要求进行以下必要的临床实验室检查,以排除任何严重疾病:血常规、尿常规以及肝肾功能。试验结果将被记录下来,以评估试验的安全性。CRF记录与治疗相关的不良事件,包括局部血肿、晕厥、恶心、头晕、失眠、呕吐或腹泻,包括时间点、严重程度、采取的措施、与针灸治疗的因果关系以及最终结果。严重的不良事件将及时报告给首席研究员。
样本量计算
我们之前回顾了针灸联合多奈哌齐治疗阿尔茨海默病疗效的临床研究,以ADAS-cog为主要结局。样本量是根据我们以前的研究结果确定的。主要评价指标为ADAcog评分较基线的变化[49]发现没有使用类似干预组的随机对照研究,直到12周治疗结束。我们前期研究报道,对照组(盐酸多奈哌齐片)ADAS-cog评分降低2.32±2.02分,治疗组(针刺联合)ADAS-cog评分提高4.04±4.23分。采用NCSS-PASS V11.0.7(5%显著性水平,90%效度,μ1 =2.32, μ2 = 2.02, δ1=4.04, δ2= 4.23, 1-β = 0.9)分析上述数据(μ1 =2.32, μ2 = 4.23, 1-β = 0.9)https://www.ncss.com/software/pass/),结果发现每组大约需要80名参与者。考虑到15%的退出率以减少偏见,至少需要184名参与者。
招聘
参与者将通过互联网和健康报纸从上海的三家医院招募。关于预防和治疗阿尔茨海默病的科学讲座将在社区服务中心举行。此外,参加者将被邀请到一个固定地点与研究联络员面对面会面,以评估资格标准。3个月内未做核磁共振的患者将重新检查。在获得知情同意并填写研究病历后,患者将接受静脉穿刺基线评估。将根据评估和检查结果决定是否纳入患者。这项研究将包括184名患者。
分配
序列生成
将使用中心随机化方法。随机数由龙华医院数据管理中心专人通过统计软件SPSS (IBM SPSS统计版本22.0,USA)网络统一发布。这可以确保隐藏随机分配。
分配隐藏机制与实现
点胶顺序密封在一个不透光的信封里,有一个唯一的识别号码。信封将被发送给一个专门的调查员,他将在何时和谁打开信封上写回信。此识别号码将作为参与者的代码出现在所有报告表格上。在研究过程中,由不同的研究专家分别进行序列生成与分配、招募、中医辨证、针灸治疗、疗效评价、数据管理、统计分析等工作。
基础垫层
在本研究中,由于干预的性质,医生和针灸师不会因分组手术而失明。数据评估将由两名不知道分组的评估人员进行。数据收集和统计分析由第三方完成。因此,除了两组之间的待遇差异外,所有参与者都将得到尽可能平等的待遇。在干预过程中,针灸师的治疗和评估者量表的评估将在不同的时间进行,以确保他们之间不能相互交流。
数据收集和管理
所有数据将由评估员在个案报告表(CRF)上进行更正,然后由两名专职人员在电子管理系统中进行双重录入。评估人员与数据录入人员在研究开始前签订保密协议,数据不得泄露。研究发起人应在研究结束后保留CRF 5年。
伦理批准并同意参与
本研究方案和研究同意书由龙华医院伦理审查委员会(2018LCSY060)、华山医院伦理审查委员会(2018-434)和上海市精神卫生中心伦理审查委员会(2018-72)批准。
在参与任何与研究相关的干预之前,每位参与者都将提供书面知情同意书。在签署同意书之前,参与者将被告知所有的研究程序、好处和风险。此外,患者将被告知参与项目是自愿的,他们可以随时退出。将患者在脱落前收集的数据纳入有意分析。从退出研究的参与者获得的数据将包括在分析中,以确定结果。在签署知情同意书之前,所有参与者都不会接受干预。
质量控制
在参与本研究之前,所有调查人员都必须参加并通过培训课程,特别是评估量表和疾病诊断(由上海阿尔茨海默病及相关疾病中心进行)的评估将由对分组分配不知情的个人进行。各医院由独立的中医医师进行辨证。辨证针灸方案培训由上海中医药大学龙华医院提供。
监督和监测
数据监控
电子数据管理系统由中国中医科学院基础研究所开发,用于收集和管理数据。
上海市科学技术委员会将成立一个独立于研究人员的专家组,对该项目进行年度评估。项目组成立三级监督委员会,定期对成果评估和数据管理进行监督
协议的修正案
上海中医药大学附属龙华医院伦理委员会将进行随机抽查,以确保研究符合方案要求。如果研究方案有任何变化,将在临床注册方案中上报伦理委员会批准并及时修改。
传播策略
这项研究的结果将发表在同行评议的期刊上。与会者可以要求对结果进行总结。
患者和公众参与声明
患者和公众不参与试验的设计和实施。也没有让患者参与结果报告或传播的计划。
统计方法
所有统计分析将使用SPSS Statistics for Windows V21.0 (IBM SPSS)进行。将使用三组数据:
- (1)
全分析试验(FAS)。这将包括所有接受至少一次疗效分析评估的随机病例。数据缺失可能会影响分析,将使用上次观测数据进行补充。FAS将是疗效评价的主要人群。
- (2)
协议集(PPS,每个协议集)。这将包括符合试验方案中规定的纳入标准,完成所有观察期计划,并且在试验期间未使用其他可能影响疗效评估的药物或治疗措施的患者。使用FAS和PPS进行疗效评价。PPS是疗效评价的次要人群。
- (3)
安全分析数据集(SS,安全集)。这将包括所有至少使用过一次研究药物并在随机分组后进行治疗后安全性评估的病例。SS将是安全评估的主要人群。
所有统计检验均为双侧进行,统计显著性设为p< 0.05。定量指标将使用均值和标准差、最大值、最小值和中位数来描述;此外,分类指标将用数字和百分比来描述。对于计数数据,两样本检验(包括Cochran-Mantel-Haenszel检验)或Fisher精确概率法将用于组间比较;此外,测量数据将表示为平均值和标准差。组间比较将使用单向方差分析;此外,组间比较将采用最小显著性差异法(LSD-t检验)。
人口统计学(年龄、性别、患病时间、教育程度)和MMSE分数将在两组之间进行比较,作为基线评估。疗效评估的主要时间点是治疗12周(PPS),以及停药时间(FAS人群)。的t-test将用于其他测量疗效指标的组间比较,包括分析与基线相比的变化。ADAS-cog、MMSE、ADCS-ADL和QOL-AD将使用协方差分析模型与基线进行组间比较。