摘要
背景
自2020年冠状病毒爆发以来,仅欧洲就有270多万名covid -19感染者住院治疗。针对SARS-CoV-2的干预措施仍然非常需要,以防止世界各地的icu住院。FX06是人类和其他哺乳动物中天然存在的肽,具有通过改善内皮功能障碍从而防止患者病情恶化来减少毛细血管泄漏的潜力。通过IXION,我们希望调查FX06在住院、非插管的COVID-19患者中预防疾病进展的潜力。
方法
IXION是一项欧盟范围内的多中心、安慰剂对照、双盲、平行、随机(2:1)II期临床研究。患者招募将于2022年9月(至2023年第二季度)在德国、意大利、立陶宛、西班牙、罗马尼亚、葡萄牙和法国开始。共纳入306例SARS-CoV-2 PCR检测阳性、COVID-19严重程度按WHO分级为4-6级的住院患者(≥18岁,< 75岁)。在随机分为FX06组或安慰剂组后,患者将接受评估至第28天(并随访至第60天)。FX06 (2 × 200 mg / d)或安慰剂静脉注射,连续5天。主要终点是证明接受FX06的患者与接受安慰剂的患者在疾病进展/恶化的患者比例上存在差异。次要终点为肺功能、氧饱和度和呼吸频率、全身炎症、生存期、毛细血管再充盈时间、住院时间和药物责任。
讨论
通过IXION,这个多学科联盟的目标是在针对SARS-CoV-2的标准护理之外,为COVID-19轻、中度阶段的临床管理提供一种新的治疗方法。潜在的限制可能是指由于各种可能违反协议而缺乏招募和退出。虽然我们在相同规模的估计中控制了辍学率,但招聘问题可能会受到难以控制的外部问题的影响。
试验注册
EudraCT2021-005059-35.于2021年12月12日注册。研究代码TMP-2204-2021-47。
背景
设置
SARS-CoV-2,正式名称为严重急性呼吸综合征-冠状病毒2 (SARS-CoV-2),对全球卫生保健系统构成了未知的挑战。该病毒传染性强,即使在无症状期也能传播,毒力相对较低,因此迅速跨地理区域传播,引发大流行[1].2019年12月8日,湖北省出现首例新冠肺炎确诊病例[2].从那时起,这种感染在全球范围内蔓延,有近4.33亿例确诊病例和600万人死亡(世界卫生组织2022年3月8日的情况报告)[3.].
COVID-19的主要临床症状为呼吸道受累,从轻度流感样疾病到可能致命的急性呼吸窘迫综合征或暴发性肺炎[1].SARS-CoV-2与其他冠状病毒具有相似的特征,包括表面具有尖突的球形形态以及高度的序列同一性,例如与SARS-CoV和sars样冠状病毒(SL-CoV) [4].与SARS-CoV相比,SARS-CoV-2的致病性较低,但具有较高的人际传播能力[5].
新冠病毒感染后出现严重的肺泡损伤,这可能是由于肺的肺泡细胞(II型)更容易被新冠病毒感染所致[6].SARS-CoV-2通过血管紧张素转换酶2 (ACE2)作为细胞受体感染宿主细胞。这种膜结合的氨基肽酶受体主要在人体内的心脏、肠、肾、肺泡细胞等各种组织中表达,并在内皮细胞上普遍存在[7].ACE2可以抵消血管紧张素II的活性,防止ACE系统的有害激活。据推测,ACE抑制剂和血管紧张素受体阻滞剂(arb)可能会增强ACE2的表达,从而导致COVID-19进展更严重[8].SARS-CoV-2已被证明能够直接进入体外工程的人血管类器官[9].各种血管床微循环功能的全身性损害可能是由sars - cov -2诱导的内皮炎所解释的,这也可能是严重COVID-19患者临床灾难性病程的原因之一[10].
对患者,特别是中重度COVID-19患者的用药取决于潜在的病理特征和疾病的不同临床阶段。抗病毒药物(如瑞德西韦)、抗炎药(如地塞米松)、血浆和高免疫免疫球蛋白是针对COVID-19的治疗方案的一部分[11].此外,FDA还批准bamlanivimab和etesevimab联合用于患有轻至中度COVID-19的成人和儿童sars - cov -2阳性患者,这些患者有发展为严重COVID-19的风险[12].批准的用途包括治疗65岁或65岁以上和/或患有某些慢性疾病的人。bamlanivimab和etesevimab未被批准用于在SARS-CoV2感染的情况下住院或吸氧的患者,因为没有相关数据。此外,向需要高流量吸氧或机械通气的COVID-19住院患者输送bamlanivimab和etesevimab等单克隆抗体可能与较差的临床结果有关[12].
这为使用抗炎药物(如抗细胞因子定向药物,如托珠单抗)稳定内皮提供了理由。COVID-19引起严重的细胞因子风暴,随后出现水肿、毛细血管渗漏综合征,从而导致肺和其他器官功能障碍[13].
目前仍缺乏治疗方案,对COVID-19患者有效和安全疗法的医疗需求很高。
FX06是一种天然存在的肽,可能是改善内皮功能障碍、毛细血管渗漏、动脉氧合和肺功能的一种有前途的创新策略,并可能能够预防疾病进展。
在一个病例报告中,FX06被用于减少埃博拉感染患者的毛细血管渗漏综合征和改善肺功能。服用FX06后,血管渗漏综合征和呼吸参数得到显著改善。此外,埃博拉病毒特异性抗体的检测伴随着病毒载量的下降[14].
在德国两所三级保健大学医院,6名在ICU入院时患有中重度ARDS并机械通气的COVID-19患者接受了静脉注射FX06 (400 - 600mg / d;3-7天)作为COVID-19重症患者择期抢救治疗的一部分[15].患者年龄在51 ~ 78岁之间;所有患者都至少有一种共病(如肥胖、2型糖尿病、支气管哮喘),所有患者都需要有创通气。在他们的疾病过程中,这6名患者中有5名需要额外的ECMO治疗。在FX06开始给药后的前3天,平均氧合比有所改善,恢复到基线水平,然后从第7天开始稳定上升。
在一项II期研究中,234例急性心肌梗死患者接受了剂量为400mg的FX06静脉注射,间隔10分钟,分为两次大剂量注射。经MRI评估,FX06治疗后5天坏死区域显著减少。接受FX06治疗的患者也表现出死亡率和任何心脏事件的联合临床终点改善的趋势。与安慰剂组相比,fx06治疗组发生的严重心脏事件数量较少,不良事件没有差异[16].
FX06可能是改善内皮功能障碍、毛细血管渗漏、动脉氧合和肺功能的一种创新策略,可能能够预防疾病进展。
方法
该研究的计划与SPIRIT声明指南一致,以确保研究的完整报告[17].研究方案V1.1 (EudraCT号;2021-005059-35)、患者信息和知情同意于2022年2月18日由德国法兰克福大学伦理委员会(编号:2021-512-AMG,主席:Dr. Harder教授)和所有参与中心批准。同时,该研究文件已根据§42 Abs. 2 AMG和§9 GCP-V的要求获得了相关联邦机构(Bundesinstitut für Arzneimittel und Medizinprodukte - No. 61-3910-4045190)的批准。每位患者必须书面知情同意才能参加研究。
对正在进行的研究的议定书修改必须通过修正案进行,并将通过欧盟进行通报。发起人有责任获得联邦监管机构对修订的独立批准,并根据GCP要求获得主管道德委员会的积极意见。如果适用,必须将修订通知监管机构。主办方将准备一份完整的、完整的最终临床研究报告。本报告将由本研究的协调研究员签署。调查人员每人将收到一份本报告的副本。
出版物将根据标准指南编写,作者身份在内部确定,并根据作者身份指南(例如,良好出版规范和医学期刊学术著作的行为、报告、编辑和发表建议)确定。
试验设计
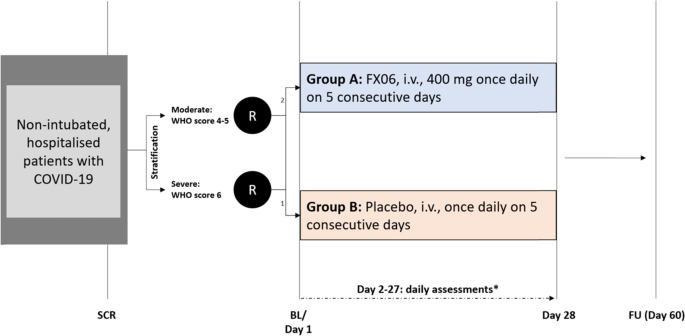
IXION将是一项欧盟范围内、多国、安慰剂对照、双盲、平行、随机(2:1)的II期临床研究,旨在调查FX06与标准护理相比在预防住院非插管COVID-19患者疾病进展方面的优势。总共306名符合纳入标准的患者将根据其WHO严重程度分组(中度:评分4-5或严重:评分6)进行分层,并由中心随机2:1分为两个治疗组(FX06或安慰剂)。1).
由于跨国设计,患者将在德国、意大利、立陶宛、西班牙、罗马尼亚、葡萄牙和法国招募。
参与者
在本研究中,我们将研究FX06在住院、非插管的COVID-19患者中预防COVID-19进展的潜力。我们还将研究对SARS-CoV-2阳性住院患者病情改善、肺功能、内皮功能障碍、毛细血管渗漏和动脉氧合的影响。因此,在本研究中,住院的非插管COVID-19患者将在5天内接受FX06(除标准护理(SoC)外)或安慰剂(除SoC外)。对患者的观察将持续到第28天(并在第60天进行随访)1).
患者和潜在研究参与者由临床合作伙伴的研究中心确定,并根据以下标准纳入研究:
入选标准
新型冠状病毒感染经PCR检测确诊
住院病人
WHO得分4-6
室内空气氧饱和度≤92%
每分钟呼吸次数≥20次
≥18岁,< 75岁
患者在开始任何协议要求的程序之前获得的书面知情同意
愿意遵守研究程序和研究方案
患者能够理解研究要求并给予书面知情同意
排除标准
重要的已知潜在合并症或病症,定义为:
其他严重晚期或慢性肺部疾病(如COPD Gold≥III,严重矽肺)
终末期慢性肾病(第5期)
终末期慢性心力衰竭(NYHA≥III)
痴呆
基线神经系统疾病排除了康复的可能性
弥散性和/或转移性恶性肿瘤
根据治疗医师的意见,病情严重,预期寿命少于6个月
Immunocompromized患者:
- 我。
接受实体器官移植的人
- 2
因自身免疫性疾病(如生物制剂)而定期服用抗炎药物
- 3
原发性免疫缺陷
- 我。
其他重大未控制的伴随疾病或严重和/或预后不良的未控制疾病的证据,可能会干扰对患者安全性的评估和治疗医师判断的研究结果
孕妇或哺乳期妇女
具有生育潜力的男性或女性在研究期间不愿意采取有效的避孕措施
目前参加过另一项IMP介入临床试验或在过去30天内参加过
干预试验药物FX06
FX06是人类和哺乳动物中天然存在的肽Bβ15-42,来源于纤维蛋白的E1片段。FX06的作用机制是认识急性炎症和水肿形成的重要新发现。FX06与纤维蛋白的E1片段竞争与内皮特异性分子VE-cadherin的结合,从而发挥抗炎作用,并通过VE-cadherin发出信号,从而减少血浆渗漏到组织[16,18].基于血管渗漏和全身炎症的动物模型,FX06对与血管通透性增加相关的所有疾病和病理状况具有相当大的治疗潜力[19,20.].FX06与血管内皮细胞(VE)-cadherin结合,阻止VE-cadherin依赖的白细胞转运[21].除了许多不同的休克动物模型(脓毒性、出血性、低血容量)外,FX06还在大鼠、小鼠和猪的急性和慢性心肌缺血和再灌注损伤模型中进行了测试[18] [20.,22].FX06使相对梗死面积减少40%以上;这种效应大小与缺血预处理相当。该肽合成用于外源性人给药[21].FX06在I期研究中耐受良好[21].
FX06已在一项IIa期临床试验中对首次接受原发性经皮冠状动脉介入治疗的急性STEMI (st段抬高心肌梗死)患者进行了评估。在这项概念验证试验中,FX06在磁共振成像上减少坏死核心区作为梗死面积的一种测量方法,并表现出安全性和良好的耐受性。
此外,FX06已在一个埃博拉病毒感染的严重病例中进行了富有同情心的使用。病人病重后痊愈,并无提出药物相关的安全问题[21].
法国的一项研究人员发起的试验(IIT)在IIa期研究中使用研究产品FX06/安慰剂治疗重症COVID-19机械通气患者。2020-002056-20)。
由于在法国/巴黎的FX06 II期IIT研究中没有安全问题,在该研究中FX06静脉注射5天(2 × 200 mg / d),因此决定使用相同的给药方案。
随机化
随机列表将由授权人员通过主办方生成。将以2:1的比例分配FX06和安慰剂,按WHO组(中度:评分4-5分,重度:评分6分)和中心分层。作为随机化过程,将采用分层块随机化。随机分组将在eCRF系统开放诊所内集中进行。独立药剂师将根据计算机生成的随机列表分发分配的治疗。
分配
随机化列表不适用于盲法研究人员,包括治疗医师。在临床中,通过为FX06提供安慰剂IMP来隐藏治疗分配,与研究药物相比,FX06将具有相同的外观。
实现
随机化序列由数据管理在研究开始前生成并验证。符合条件的患者由研究人员登记,研究人员根据计算机生成的随机化列表将患者分配到下一个随机化治疗。按随机数给予盲法IMP。
基础垫层
该研究是随机的,对受试者、治疗师和评估人员进行盲法(双盲法)。在整个研究过程中,治疗分配仍然隐藏,以最大限度地减少评估和选择偏倚和评估偏倚的风险。
在最终分析之前,研究统计学家对治疗分配也保持盲法,以避免早期数据驱动的结论。
研究目标
主要目标和终点
主要目的是证明接受FX06的患者与接受安慰剂的患者在28天之前病情进展/恶化的患者比例的差异。
两治疗组患者病情恶化至28天的比例
疾病状态进展/恶化定义为连续3天WHO评分恶化(始终与BL WHO评分相比较),直到第28天(例如,BL WHO评分为4的患者连续3天WHO评分为5,则定义为疾病恶化)
WHO评分对疾病严重程度和进展的评估是根据WHO的建议选择的[23将这一分数纳入所有COVID-19临床试验。此外,对于这项国际性的多中心研究,它促进了跨研究中心疾病严重程度的可比性和客观评估。
次要目标和终点
FX06组和安慰剂组在所有可用的访问和时间点对以下目标进行评估和治疗比较:
疾病进展/改善(世卫组织量表评分)
病情好转或进展的患者比例
每种WHO评分的患者比例
WHO得分与BL相比的平均变化
WHO平均得分
每种疾病严重程度(未感染、轻度、中度、严重、死亡)的患者比例
需要机械通气的患者比例及通气天数
需要ECMO的患者比例和ECMO天数
肺功能(分氧压、吸入氧分数、霍洛维茨指数)
PaO2绝对值(mmHg)及与BL相比的变化
绝对FiO2 (mmHg,吸入氧分数)及其对BL的变化
霍洛维茨指数(mmHg),改为BL
(肺功能评估只有在常规进行时才会记录在研究中)
氧饱和度和呼吸频率
氧饱和度、呼吸频率和BL变化
在室内空气中达到92%氧饱和度的患者比例
全身炎症(肌钙蛋白、降钙素原、CRP、白细胞计数、铁蛋白、d -二聚体、乳酸、乳酸脱氢酶、白蛋白的改变和正常化)
血液参数浓度及其对BL的变化
全身炎症恢复正常的患者比例(针对各个炎症参数)
生存
存活至28天的患者比例
存活到60天的患者比例
毛细血管再充盈时间
基线时毛细血管再充盈时间正常和病理(病理:≥2 s或正常:<2 s)并发生BL变化的患者比例
住院时间
住院至第28天或第60天的天数
出院至第28天和第60天的患者比例
药物问责制(例如剂量、给药次数)
IMP管理数量
平均每日IMP剂量和平均累积IMP剂量
SARS-CoV-2 rt - pcr ct值和至阴性时间(即由每个当地实验室定义的连续两次pcr检测阴性)
呼吸道标本SARS-CoV-2 RT-PCR阴性时间
第6天、第10天和第28天SARS-CoV-2 PCR检测阴性患者的比例
SARS-CoV ct值的变化(减少)
亚组分析:伴随用药和SARS-CoV-2疫苗接种情况
我们描述了治疗组的亚组分析。我们也保留权利在两组之间用探索性统计检验进行比较。
探究的目的
毛细管泄漏评估(血浆ADM)
血浆ADM量及BL变化
血浆表型:内皮功能障碍和免疫特征
血管性血友病因子(vWF)、纤溶酶原激活物抑制物-1 (PAI-1)、ICAM-1、VCAM-1、e -选择素含量及BL变化
Il-1α, il-6, il-10
组学分析侧重于免疫参数
生活质量、医疗保健使用和生产力
第28天和FU的EQ5D-5L评分(也是单题)
在FU评估医疗资源的使用和生产力
安全
安全参数(为安全集进行评估)
不良事件和严重不良事件数
(严重)不良事件的类型和严重程度(轻、中、重)
(S)不良事件的严重性和相关性
注射IMP后1小时内,平均每位患者发生与注射相关的AEs (S)数
治疗相关的AEs(年代)
无论患者接受何种治疗,任何严重的临床不良事件或实验室检测值异常都必须由研究者在知情24小时内报告给主办方。我们使用当地药品法、GCP和ICH临床安全数据管理指南的定义和报告要求。由于生存/死亡是一个终点参数,当报告致命和/或危及生命的susar系统地打破盲法时,临床试验的完整性可能会受到损害。因此,符合以下标准的致命和/或危及生命的急性急性呼吸道疾病将被视为与疾病相关,不需要进行系统的盲检和快速报告:
血液动力学的恶化
肝细胞溶解/不足
急性肾功能衰竭
弥漫性血管内凝血/出血
白细胞减少、血小板减少症、贫血
严重肠系膜缺血
脑死亡/出血性中风/缺血性中风
肺栓塞
急性心肌梗死/心律失常
吸入性肺炎/呼吸机获得性肺炎/菌血症/真菌血症
不良事件,特别是那些与测试“药物”有“相关”关系的不良事件,应随访直至解决或直至FU就诊。如果有明确的解释,应记录在CRF上。ae的治疗由研究者自行决定,并应遵循研究者所在机构的医疗护理标准。
保险
保险承保不迟于在投保人身上进行的临床试验结束后10年发生的健康损害,并在不迟于临床试验结束后10年报告给保险公司
学习管理小组
IXION被嵌入欧盟成立的项目COVend中。因此,根据大协议,欧盟项目所需的基础设施(如指导委员会和数据管理器)将用于IXION。为确保最高安全水平,我们成立了外部科学顾问委员会、风险评估小组、数据安全监测委员会和道德顾问委员会。
数据安全监察委员会
为了这项研究,政府将成立一个数据安全监察委员会。DSMB是一个独立的专家咨询小组,其任务是定期审查盲法和非盲法安全性数据,以便对试验的效益和风险进行持续判断。如果DSMB确定该研究不符合必要的安全性要求(例如,有新的信息使收益-风险平衡变为负的),则DSMB可以建议停止、暂时中止或修改该研究。DSMB由在临床研究中具有临床和科学专业知识的医生和科学家组成。
为了确保高水平的数据安全,项目建立了GDPR数据保护概念。此外,所有参与伙伴也必须有数据保护的概念。更多信息可以在相应的数据保护概念中找到。
数据访问
在研究过程中,医学研究人员当然可以访问eCRF(使用化名数据),以及数据管理人员、监测人员、实验室工作人员、项目管理办公室、赞助商和项目管理人员(都对研究药物不知情)。药物安全医生和DSMB应要求或在DSMB会议之前从数据库中获得所需的安全摘录,并有可能在必要时解除治疗数据的盲。血浆表型的实验室结果(ITMP实验室)每月以CSV格式传输,经数据管理转换为XML格式后导入研究数据库。统计人员收到研究数据进行评估,研究完成后,发起人收到全部假名数据,调查人员收到各自研究中心的数据(关于数据载体的pdf文件)。在任何情况下,只传递匿名数据。
在研究期间,除研究中心的研究人员外,只有主办方的授权代表(如CRAs和审核员)和负责的监测机构有权访问个人健康数据(研究中心的患者档案)。
研究结束后,收集的数据和生物标本不再计划进行进一步的研究。
样本量的考虑
根据我们的文献研究[24,25,26],我们估计在安慰剂下病情没有恶化的患者(+SoC)的频率为70%,因为我们只包括住院的COVID-19患者,而不包括任何病情轻微的流动COVID-19患者。我们预计FX06 (+SoC)将这一速度提高约15%。根据Spinner等人和法兰克福KGU ICU的估计,我们还预计FX06治疗组(+SoC)与安慰剂治疗组(+SoC)相比,病情进展/恶化的患者减少15%。
应用一个Z-连续校正后显著性水平为5%的比例检验,n= 291例患者(194 FX06: 97安慰剂;(没有退出),需要证明疾病进展/恶化患者比例在第28天的治疗差异为80%。考虑到5%的退出,需要招募306名(204 FX06: 102名安慰剂)患者。
使用G*Power 3.1.9.6版本计算样本量Z-测试两个独立比例之间的差异,并进行连续性校正。使用PASS 16.0.2重新确认样本量。
统计方法
统计分析将在研究结束后,当所有纳入患者完成最后一次就诊,数据管理的数据审核流程完成,数据库硬锁定,所有数据查询解决后,由研究统计员进行统计分析。在数据库被硬锁定后,数据将被解除盲化。下面是应用方法的简短总结。详细的描述将在提供附加文件.
用于分析的总体定义
根据纳入和排除标准,纳入符合条件的住院非插管COVID-19患者。
所有随机纳入的患者(RS,随机组)
随机集(RS)的定义包括所有随机参与研究的患者。请注意,只有当患者未服用至少一剂药物(除RS外,这些不属于分析集的一部分)和/或患者撤回同意和/或研究者/PMO/主办方将患者从研究中撤回时,才会出现随机患者退出的情况。如果患者从IMP中退出,他们不会退出研究,因此仍然是分析集的一部分。
全分析集(FAS)
对于主要和次要目标最终分析的完整分析集(FAS),我们将只考虑所有随机纳入患者(RS)的亚组,这些患者基于who评分对其疾病状态进行了基线和一次基线后评估,并且在研究期间至少接受了一次FX06/安慰剂剂量。否则,在使用IMP的情况下,不能估计考虑的主要终点和治疗效果。注意,FAS可能等于RS。
按方案人口
每个方案人群(PP)被定义为FAS的子集,不包括发生到28天的严重违反方案的患者。排除的具体原因将在数据库关闭之前记录在案。并非所有协议偏离者和违规者都将被排除在每个协议种群之外。
Safety-population
安全性分析集定义为所有在研究期间接受至少一剂FX06/安慰剂的随机患者。该人群是所有随机纳入患者(RS)的一个子集,将用于所有安全性分析。
辍学生
只有当患者未服用至少一剂药物(除RS外,这些不属于分析集的一部分)和/或患者撤回同意和/或研究者/PMO/主办方让患者退出研究时,才会出现随机患者退出的情况。
如果患者从IMP中退出,他们不会退出研究,因此仍然是分析集的一部分。
我们希望病人有很高的内在动力。IXION是一项II级医学研究,由专业研究中心在监测监督下进行。此外,患者的学习负担也尽可能低,例如,临时访问可以远程进行。
缺失值
我们不期望由于接近的访问窗口和病人护理而有许多常规的缺失值。收集到第28天的世界卫生组织评分将受到严格控制。通常,除非另有说明,否则参数的实际缺失数据将不会被转换并保持不变。将提供汇总统计数据,包括有效个人值的基础数量和缺少访问。
我们预先定义以下处理所选分析数据的方法:
所有在第28天之前死亡的患者,在其死亡评估访视时及之后的所有剩余访视中,将被给予相应的who最高评分(评分为10),以评估主要终点和相关敏感性分析,即使在死亡访视后无法收集进一步的患者数据。死亡日期将被视为事件时间分析的时间点。如果在第28天前退出或在第28天前FAS人群的WHO评分缺失,如果主要终点的统计推断可能独立于WHO评分缺失,则将进行评估,例如,因为患者在某一时刻显示WHO评分恶化,或连续就诊不超过3次显示WHO评分恶化。如果无法推断主要终点,则可以通过在盲法数据审查会议上对这些病例进行更仔细的研究来推断WHO评分缺失的决定,在盲法数据审查会议上,对患者的所有可用信息进行盲法评估。所有剩余的无法分配WHO评分的FAS患者将被认为缺席初步分析,并将被不同的场景视为初步分析的敏感性分析(最佳/最坏情况场景和LOCF)。对于所有进一步的端点,目前没有计划进行归责。
请注意,使用最大似然估计的线性混合模型能够处理缺失值,是一种有效的imputation替代方案。因此,实验室评估预计将根据lmm中的缺失准确建模。
除非另有说明,低于或高于最低限量的值一般会根据化验值的性质及其评估时间,以适当的固定值(例如最低限量、最低限量、零)计算。如果实验室参数的大量测量值高于/低于限量,则将考虑其他方法。SARS-CoV-2抗体低于阈值(LOQ)将被定义为0/不存在,用于分析。
统计分析
作为初步分析,我们将比较两个治疗组在28天之前疾病进展/恶化(根据WHO评分定义)患者比例的差异(2样本卡方检验)。目的是证明FX06在预防疾病恶化状态方面的初步优势,与安慰剂(标准护理)治疗相比。对于组间比较,考虑5%显著性水平。
关于次要终点,将按治疗组、可用就诊次数和治疗差异分层进行总结统计,直到第28天;给出95%置信区间。对于选定的次要终点,将应用线性混合模型来调查治疗、时间、治疗时间和其他因素(如人口统计学)的影响。
讨论
偏见和限制
由于所有患者在整个治疗期间都将在医院接受治疗,我们预计在缺乏依从性方面的偏差可以忽略不计。由于我们在几个国家调查了FX06治疗下的疾病进展,当不同国家的护理质量标准不同时,可能会产生偏差。虽然这可能会影响主要终点的大小,但对主要终点治疗差异的假设不应受到影响,因为随机化可以防止不同国家在这方面的不平衡。此外,作为敏感性分析,终点将在中心之间进行描述性比较,或作为回归模型的影响。由于采用双盲研究设计,应尽量减少潜在偏差的风险。
潜在的限制可能是指由于各种可能违反协议而缺乏招募和退出。虽然我们在相同规模的估计中控制了辍学率,但招聘问题可能会受到难以控制的外部问题的影响。招募困难的一个原因是正在进行的关于COVID-19的竞争性试验,而与此同时,患者可能不想接受安慰剂治疗,尽管它代表了护理标准。
讨论
自首例报告病例以来,持续的COVID-19大流行正在影响世界各地的人们。截至2022年3月底,已报告超过4.6亿例病例和多达600万例死亡[27].
随着变体的变化和反疫苗运动,COVID-19仍然给icu带来压力。因此,我们需要新的和多样化的药物选择来治疗COVID-19。FX06靶向宿主炎症内皮可能是一种很有前途的方法。
IXION试验将回答FX06是否有可能防止COVID-19从中度到重度/危重期的进展。
此外,我们喜欢识别内皮细胞和免疫系统之间复杂相互作用的特定分子“指纹”。这可能有助于了解与内皮功能障碍和毛细血管泄漏有关的其他疾病(例如败血症和急性呼吸窘迫综合征)。
试验状态
研究方案(V1.1)于2022年1月12日最终确定。该试验已在相关联邦机构(Bundesinstitut für Arzneimittel und Medizinprodukte - No. 61-3910-4045190)和欧盟药物监管机构临床试验数据库(EudraCT No. 4045190)注册。: 2021-005059-35)。患者招募和登记工作将于2022年底开始。招聘计划持续18个月。
数据和材料的可用性
在当前研究期间生成和/或分析的数据集可在试验结束后根据合理要求从通讯作者处获得。
缩写
- ACE2:
-
血管紧张素转换酶2
- AE:
-
不良事件
- ALT:
-
丙氨酸转氨酶
- ARDS:
-
急性呼吸窘迫综合征
- AST:
-
天冬氨酸转氨酶
- bio-ADM:
-
生物活性Adrenomedullin
- 提单:
-
基线
- 体重指数:
-
身体质量指数
- C:
-
浓度
- 置信区间:
-
置信区间
- 肤色线:
-
间隙
- 慢性阻塞性肺病:
-
慢性阻塞性肺疾病
- COVID-19:
-
2019冠状病毒病
- c反应蛋白:
-
c反应蛋白
- CRT:
-
毛细血管再充盈时间
- ct:
-
循环阈值
- DMP:
-
数据管理计划
- 例如:
-
例如;例如
- ECMO:
-
体外膜氧合
- 供给:
-
吸入氧分数
- 傅:
-
后续
- 质量:
-
良好临床实践
- 包含:
-
粒细胞集落刺激因子
- GGT:
-
Gamma-glutamyl转移酶
- GMP:
-
良好医疗规范
- 你好:
-
霍洛维茨指数
- 静脉输液/ IV:
-
静脉注射
- AEs (S):
-
(严重)不良事件
- ICAM-1:
-
细胞间粘附分子
- EQ-5D-5L:
-
患者报告结果(PRO)-仪器
- 加护病房:
-
重症监护室
- 免疫球蛋白:
-
免疫球蛋白G
- 个人所得税:
-
研究者发起的审判
- IL:
-
白介素
- 小鬼:
-
临床试验药品
- IUD:
-
子宫内的设备
- 核磁共振成像:
-
磁共振成像
- SoC:
-
护理标准
- 可控硅:
-
筛选
- STEMI:
-
st段抬高型心肌梗死
- 人:
-
世界卫生组织
参考文献
心血管疾病和COVID-19。糖尿病代谢综合征,2020;14(3):247-50。
吴震,McGoogan JM。中国2019冠状病毒病(COVID-19)暴发的特征和重要教训:中国疾病预防控制中心72314例病例报告摘要《美国医学协会杂志》上。2020; 323(13): 1239 - 42。
谁。COVID-19流行病学每周更新。第82版,2022年3月8日出版;2022.
田旭,李超,黄安,夏松,卢松,史志,等。SARS冠状病毒特异性人单克隆抗体与2019新型冠状病毒刺突蛋白的有效结合。新兴微生物感染。2020;9(1):382-5。
李强,关旭,吴鹏,王旭,周林,童勇,等。新型冠状病毒感染的肺炎在中国武汉的早期传播动态中华实用医学杂志,2015;29(4):529 - 529。
齐健,周勇,华健,张玲,边娟,刘波,等。受体ACE2和细胞蛋白酶TMPRSS2的scRNA-seq表达谱揭示了易感染SARS-CoV-2的人体器官。《国际环境与公共卫生杂志》,2021;18(1):284。https://doi.org/10.3390/ijerph18010284.
李志强,李志强,李志强,等。假定的SARS-CoV-2受体ACE2在人类心脏中的细胞类型特异性表达。欧洲心脏杂志2020;41(19):1806 -6,赖斯GI,托马斯DA,格兰特PJ,特纳AJ,霍珀NM。血管紧张素转换酶(ACE)及其同源物ACE2和奈普利利素在血管紧张素肽代谢中的作用。生物化学学报(英文版);2004;29(1):1 - 5。
Mehra MR, Desai SS, Kuy S, Henry TD, Patel AN。心血管疾病、药物治疗和Covid-19的死亡率。中华实用医学杂志,2015;29(2):344 - 344。
孟伟伟,李志强,李志强,等。使用临床级可溶性人ACE2抑制工程人类组织中的SARS-CoV-2感染。细胞。2020;181(4):905-13 e7。
张志刚,张志刚,张志刚,张志刚,等。COVID-19的内皮细胞感染和内皮炎。柳叶刀》。2020;395(10234):1417 - 8。
Stasi C, Fallani S, Voller F, Silvestri C. COVID-19治疗综述。欧洲药物学杂志,2020;889:173644。
食品及药物管理局。冠状病毒(COVID-19)更新:FDA批准单克隆抗体用于治疗COVID-19 2021[可从:www.fda.gov新闻事件/ press-announcements / coronavirus-covid-19-update-fda-authorizes-monoclonal-antibodies-treatment-covid-19-0].
黄超,王勇,李霞,任玲,赵娟,胡勇,等。武汉地区新型冠状病毒感染患者临床特征分析柳叶刀》。2020;395(10223):497 - 506。
伍尔夫·T,康恩·G,贝克尔·S,斯蒂芬·C,布罗特·HR,德·洛乌·P,等。伴有血管渗漏和多器官衰竭的严重埃博拉病毒病:重症监护患者的治疗柳叶刀》。2015;385(9976):1428 - 35。
Adam EH, Schmid B, Sonntagbauer M, Kranke P, Zacharowski K, Meybohm P.纤维蛋白源肽Bbeta15-42 (FX06)在covid -19相关急性呼吸窘迫综合征危重患者中的挽救性治疗重症监护。2020;24(1):574。
Atar D, Petzelbauer P, Schwitter J, Huber K, Rensing B, Kasprzak JD,等。fi.r.e (FX06预防心肌再灌注损伤的疗效)试验结果:静脉注射FX06作为经皮冠状动脉介入治疗急性st段抬高型心肌梗死的辅助治疗。中华医学会心血管病杂志,2009;29(8):712 - 712。
陈伟华,特兹拉夫JM,郭澈PC,阿尔特曼DG,曼恩H,柏林JA,等。SPIRIT 2013解释和阐述:临床试验方案指南。BMJ。2013; 346: e7586。
佩策鲍尔P, Zacharowski PA, Miyazaki Y, Friedl P, Wickenhauser G, Castellino FJ,等。纤维蛋白源肽Bbeta15-42保护心肌免受缺血-再灌注损伤。中华外科杂志,2005;11(3):298-304。
Bergt S, Gruenewald M, Beltschany C, Grub A, Neumann T, Albrecht M,等。纤维蛋白来源的肽Bbeta15-42 (FX06)改善血管渗漏,提高生存和神经认知恢复:心肺复苏的两个动物模型的意义。张志勇,张志强,张志强,等。重症监护医学杂志,2016;44(10):e988-95。纤维蛋白切割产物Bbeta15-42在小鼠肾缺血再灌注损伤急性后过程中促进内皮细胞和小管再生。9:369, Wiedemann D, Schneeberger S, Friedl P, Zacharowski K, Wick N, Boesch F,等。纤维蛋白衍生肽Bbeta(15-42)在心脏移植模型中显著减弱缺血-再灌注损伤。移植。2010;89(7):824 - 9。
郭志刚,王志刚,王志刚,王志刚,等。肽Bbeta(15-42)保护休克时内皮屏障功能。公共科学学报。2009;4(4):e5391。
台塑。专营。调查员手册:FX06(肽Bß15-42)。版没有。3.2:第84页,2021年4月。
罗斯纳,裴泽鲍尔,柯赫,陈恩,伊伯,穆茨,等。一项双盲、单中心、亚慢性再灌注试验,评估猪出血性休克后FX06。复苏。2009;80(2):264 - 71。
特点WHOWGotC,管理C-i。COVID-19临床研究的最低通用结果测量标准。《柳叶刀》感染杂志2020;20(8):e192-e7。
管文杰,倪志勇,胡勇,梁文华,欧常青,何建新,等。2019年中国冠状病毒病临床特征王东,胡斌,胡超,朱峰,刘霞,张娟,等。武汉市138例新型冠状病毒感染的肺炎住院患者临床特征分析《美国医学协会杂志》上。2020年,323(11):1061 - 9。
Spinner CD, Gottlieb RL, Criner GJ, Arribas Lopez JR, Cattelan AM, Soriano Viladomiu A,等。瑞德西韦与标准治疗对中度COVID-19患者11天临床状态的影响:一项随机临床试验《美国医学协会杂志》上。2020年,324(11):1048 - 57。
李志强,李志强,李志强,等。bamlanivimab单独治疗或联合etesevimab对轻中度COVID-19患者病毒载量的影响:一项随机临床试验《美国医学协会杂志》上。2021年,325(7):632 - 44。
Dong E, Du H, Gardner L.实时跟踪COVID-19的交互式web仪表板。《柳叶刀》感染杂志2020;20(5):533 - 34。
确认
IXION合作小组将作为一个作者列出,并且可以通过他们的个人出版记录搜索小组成员的名称:
德国美因河畔法兰克福歌德大学法兰克福大学医院麻醉科、重症监护医学和疼痛治疗科
Oliver Old, Markus Ketomaeki, Lea Grebe, Patrick boom, Simone Lindau, Sebastian Zinn, Isabel Maushagen
德国美因河畔法兰克福歌德大学法兰克福大学医院内科、传染病科
提莫·沃尔夫,克里斯托弗·斯蒂芬
欧洲麻醉学和重症监护学会(ESAIC),布鲁塞尔,比利时
凯西·维纳特,西尔维娅·达曼
F4 Pharma GmbH,维也纳,奥地利
佩特拉Wülfroth,托马斯·斯坦纳
荷兰格罗宁根Martini医院临床药学和毒理学科
荷兰格罗宁根大学医学中心健康科学系
Marinus van Hulst
德国维尔茨堡大学医院麻醉科、重症监护、急诊和疼痛科
Peter Kranke, Sebastian Hottenrott, Tobias Schlesinger, Benedikt Schmid, Daniel Röder, Eva Kranke, Tobias Haas, Philipp Schlesinger, Magdalena Sitter
意大利佩鲁贾大学医学与外科学系
大卫。”
内科。贝尔维奇大学医院,巴塞罗那,西班牙贝尔维奇生物医学研究所(IDIBELL),巴塞罗那,西班牙
Raquel Torres Iglesias José María Mora-Luján, Adriana Iriarte, Pau Cerdà
立陶宛健康科学大学考纳斯医院,立陶宛健康科学大学麻醉科
Neringa Vaguliene, Andrius Macas, Jolanta Litviniene, Kristina Balne
葡萄牙科英布拉大学医疗中心
卡塔琳娜·蒙泰罗,Inês安图内斯·费雷拉,Patrícia库塞罗,佩德罗·苏亚雷斯,索菲亚Beirão
索邦大学Université, IPLESP, Hôpital圣安东尼,AP-HP,巴黎,法国
Yasmine Abi Aad, Thibault Chiarabini
“Carol Davila”医学和药学大学,麻醉和重症监护室-Fundeni临床研究所
国王Popescu
荷兰马斯特里赫特马斯特里赫特大学医学中心内科
CJH van der Kallen
赞助商
F4 Pharma GmbH(维也纳)是COVend的合作伙伴,提供临床研究材料和一般科学建议。作为财团合作伙伴,F4与其他合作伙伴一起参与了研究设计和手稿准备。根据资助与财团协议,发起人同意财团可以发表任何研究结果。
资金
由Projekt DEAL启动和组织的开放获取资金。IXION是欧盟资助的COVend项目的一部分(地平线欧洲研究和创新计划,资助协议编号为no。101045956)。
作者信息
作者及隶属关系
财团
贡献
所有作者都对本试验的概念和设计做出了重大贡献。JK、BF和KZ是本次试验的研究者,并参与了资金的获得。该研究方案是本出版物的基础,由SD、ACF和ABS起草,并由JK、BF、MV、AvA和KZ进行了审查和实质性讨论。ACF负责样本量的计算和统计方法。所有作者都参与了手稿的起草或对重要的智力内容进行了批判性的修改,并批准了最终的手稿。
相应的作者
道德声明
伦理批准并同意参与
研究方案V1.1 (EudraCT号;2021-005059-35)、患者信息和知情同意于2022年2月18日由德国法兰克福大学伦理委员会(编号:2021-512-AMG,主席:Dr. Harder教授)和所有参与中心批准。同时,该研究文件已根据§42 Abs. 2 AMG和§9 GCP-V的要求获得了相关联邦机构(Bundesinstitut für Arzneimittel und Medizinprodukte - No. 61-3910-4045190)的批准。每位患者必须书面知情同意才能参加研究。
发表同意书
不适用。
相互竞争的利益
KZ是ENVISION和COVend项目的PI,这两个项目分别获得了欧盟地平线2020和地平线欧洲研究和创新项目的资助,根据资助协议no。101015930 (ENVISION)和编号。101045956 (COVend)。所有其他作者都宣称他们没有竞争利益。
额外的信息
出版商的注意
怎么样下载亚搏施普林格自然对出版的地图和机构从属关系中的管辖权主张保持中立。
补充信息
附加文件1。
附加信息-关于IXION的进一步统计信息。
权利和权限
开放获取本文遵循知识共享署名4.0国际许可协议,允许以任何媒介或格式使用、分享、改编、分发和复制,只要您对原作者和来源给予适当的署名,提供知识共享许可协议的链接,并注明是否有更改。本文中的图像或其他第三方材料包含在文章的创作共用许可协议中,除非在材料的信用额度中另有说明。如果材料未包含在文章的创作共用许可协议中,并且您的预期使用不被法定法规所允许或超出了允许的使用范围,您将需要直接获得版权所有者的许可。如欲查看本牌照的副本,请浏览http://creativecommons.org/licenses/by/4.0/.创作共用公共领域奉献弃权书(http://creativecommons.org/publicdomain/zero/1.0/)适用于本条所提供的资料,除非在资料的信用额度中另有说明。
关于本文
引用本文
克洛卡,J.,弗里德里克森,B.,道思,S.。et al。FX06预防住院非插管COVID-19患者疾病进展的潜力——IXION的随机、全欧盟、安慰剂对照II期研究设计。试用23, 688(2022)。https://doi.org/10.1186/s13063-022-06609-x
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/s13063-022-06609-x
关键字
- FX06
- 新型冠状病毒肺炎
- 疾病进展
- 毛细管泄漏
- 炎症