摘要
背景
天然橡胶乳胶过敏是一个常见的和未解决的健康问题。由于避免暴露是非常困难的,因此强烈建议进行免疫治疗,但在对患者使用之前,必须证明提取物的有效性和安全性。
本随机、双盲、安慰剂对照临床试验的目的是评估乳胶舌下免疫疗法对永久避免使用乳胶的成年患者的疗效和耐受性。
方法
28名成年乳胶过敏患者(5名男性,23名女性),平均年龄39岁(24-57岁),随机接受一年内的商业乳胶舌下免疫治疗或安慰剂,然后再接受一年的开放、积极治疗。在基线和随访第一年和第二年结束时测量以下结果:皮肤点刺试验、手套使用评分、结膜激发试验、总IgE和特异性IgE、嗜碱性粒细胞激活试验以及不良反应监测。
结果
在疗效上没有显著差异在活的有机体内在安慰剂对照期结束时观察到活动组和安慰剂组之间的变量,在两年研究结束时将各组与基线值进行比较时也没有观察到变量。观察到嗜碱性粒细胞激活的平均百分比有所改善。在诱导阶段,记录了活性组4例和安慰剂组5例的反应。在维持期,2例患者分别因瘙痒和急性皮炎退出。
结论
需要进一步的研究来评估乳胶舌下免疫疗法,因为在避免过敏原的成年患者中无法证明疗效。
试用注册号
背景
天然胶乳(NRL)是一种普遍存在的材料,NRL过敏是一种相对较新的诊断,因为它在70年代末首次被发现[1,2].它主要影响某些高危人群(卫生保健工作者、经常住院的患者),但普通人群中乳胶致敏的患病率也不容忽视。此外,其他职业如美发师、管家、建筑工人、食物处理人员或保安人员,最近对nrl过敏的个案亦有所增加[3.,4],可能是由于广泛接触乳胶手套。因此,NRL过敏是公认的公共卫生问题,直到采取纠正措施(主要是用其他材料替代NRL或在医疗机构使用无粉手套),导致该疾病的发病率逐渐下降[5].
目前建议避免NRL以降低已确诊过敏患者过敏症状(包括危及生命的反应)的风险。然而,就NRL而言,这一措施显然是不够的,因为很难避免乳胶在许多产品中的广泛存在。由于乳胶与各种常见水果如鳄梨、香蕉或猕猴桃的交叉反应,情况也很复杂。6,7],这主要是由于Hevein (Hev b6)致敏。此外,虽然长期避免使用天然胶乳可以缓解症状,但检测到的IgE表明持续致敏超过5年[8].
假设使用NRL提取物的免疫治疗可以保护这些患者在意外接触NRL后不发生不良事件。然而,尽管它是一种常见的致敏剂,但已证明疗效和安全性的不同商业产品的可用性仍然有限。关于特异性免疫疗法的疗效和耐受性,只有少数研究发表了适当的设计(随机、双盲和安慰剂对照)。事实上,有证据表明,与安慰剂相比,皮下免疫治疗可显著改善各项疗效参数,但缺点是全身反应率高[9,10].
舌下给药的nrl免疫疗法也很少被探讨在成人患者。Patriarca等人[11]显示皮肤和呼吸道症状有改善,结膜挑战试验也有改善,但这是一项非对照研究。在另一项开放标签和非对照研究中,cstero [12]显示了比皮下途径更好的快速舌下免疫治疗的耐受性,但仅在10周后测量皮肤反应来评估疗效。Nettis发表了一项为期一年的舌下免疫治疗的双盲、安慰剂对照研究[13],在12个月的治疗后,症状和药物评分均有显著改善。最后,最近的一项试验表明,乳胶SLIT在一年的随访后比安慰剂更有效,但只有9名患者完成了研究,因此,必须谨慎对待结果[14].
考虑到舌下应用比皮下途径的耐受性更好,需要对这种疗法的长期效果进行更多的研究,特别是当这种疗法已经可用多年时。因此,我们进行了这项独立的(由研究人员赞助的)随机、双盲、安慰剂对照临床试验,以评估永久避免NRL的成年患者在市售NRL舌下免疫疗法随访2年后的疗效和耐受性。
方法
设计与伦理
这是一项独立研究,由调查人员赞助,部分资金由公共机构提供。
该研究分为两个阶段:首先,进行随机、双盲、安慰剂对照临床试验。第一年随访结束(T1),停止盲治疗,积极治疗的患者继续接受另一年的治疗(T2)。那些被纳入安慰剂组的患者以开放标签的方式接受了一年的积极治疗。
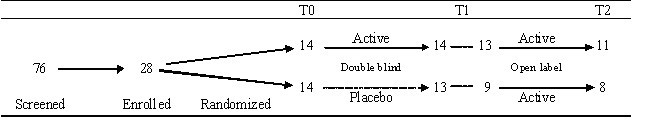
该研究得到了当地伦理委员会/独立审查委员会以及西班牙药品管理局的批准。试验根据良好临床规范进行,因此,在入组前,所有受试者在口头和书面信息的基础上给予书面知情同意,外部监测和审计由独立调查人员进行。表中总结了所有的研究过程1.
病人
在研究中心(Santiago Apostol医院,Vitoria-Gasteiz, Spain)注册的76名NRL过敏患者被提议参与这项研究。最终纳入28例患者(男性5例,女性23例),平均年龄39岁(24-57岁)。所有患者之前都被诊断为乳胶过敏,随后被指示避免接触过敏原。患者的临床特点见表2.
入选标准包括天然橡胶乳胶过敏的临床病史(记录荨麻疹、血管性水肿、鼻炎、结膜炎、哮喘或过敏反应的常见症状)或手套使用试验和/或结膜试验阳性,加上NRL(风团≥3 × 3 mm)的针刺试验阳性。排除标准包括使用免疫治疗的常见禁忌症(严重或不受控制的哮喘、其他免疫介导疾病、冠状动脉疾病或同时使用β -受体阻滞剂或血管紧张素转换酶抑制剂)[15]以及存在严重的全身性或精神疾病、慢性荨麻疹或皮肤炎。符合所有资格标准的患者被随机分配到主动免疫治疗组或安慰剂组。
研究治疗
一种市售的舌下免疫疗法(SLIT-Latex®(ALK-Abello,西班牙)在试验中进行了检测。用于试验的药物由制造商直接提供给研究中心的药剂科。它是商业批次的一部分,但按照良好生产规范指南附件XIII的规定标记为试验。SLIT-Latex®是一种含乳胶致敏提取物的盖伦配方(橡胶树取代巴西橡胶树)、人白蛋白(第4瓶除外)、氯化钠、苯酚、甘氨酸和水。根据蛋白质含量(SDS-PAGE)和总蛋白质含量对提取物进行标准化。较高浓度为500 mcg蛋白/mL。此外,安慰剂由相同的制造商制备,含有相同的成分,除了过敏原提取物。两种处理都具有相同的外观、味道和颜色。根据制造商的时间表进行免疫治疗(表3.).医生仔细指导患者将药水放在舌下3分钟后再吞下。根据EAACI的规定,出于安全考虑,诱导期在医院环境下进行,由训练有素的过敏症专家监督,每次给药后至少观察患者30分钟。连续的维持剂量在家中自行服用。患者每三个月到医院领取一次新剂量,并归还空药瓶,调查人员对这些药瓶进行计数,以评估依从性。
在活的有机体内测试
皮肤刺痛试验在每次研究访视中重复使用4种乳胶浓度(4、20、100和500 μg)。阳性(盐酸组胺10 mg/ml)和阴性(盐水溶液)对照组也包括在每个试验中。丘疹的区域被转移到纸上,然后使用特定的软件进行平面测量[16].计算了两组丘疹面积的平均值,活跃组和安慰剂组。比较免疫治疗前后针刺试验结果,计算皮肤耐受性指数(CTI)。该指标是将提取物的剂量乘以以获得相似皮肤反应所必需的因子,并估计一组相对于另一组的皮肤敏感性的大小。当用于评估一组患者是否观察到变化时,CTI高于1表示皮肤反应降低。
手套使用测试(GUT)使用高含量乳胶手套(非无菌亚琛®(西班牙)以及100%不含乳胶的乙烯基手套(Torval®,中国)。佩戴眼镜和无乳胶口罩保护患者,以避免同时发生眼部和/或吸入性暴露。患者每只手上分别戴一种手套(乳胶或乙烯基)5分钟、15分钟和30分钟,间隔20分钟。对症状(瘙痒、红斑、风疹)进行评分(0 =无;1 =轻度;2 =中度;3 =严重)如前所述[17].当症状评分达到5分时停止测试。结果表示为实现5个点的估计时间。
结膜挑战试验(CCT)使用5种浓度递增的NRL提取物(0.08 - 0.4 - 2 - 10和50 mg/ml),间隔15分钟。将低剂量的盐水滴在右眼结膜下穹窿上,将对照盐水滴在左眼上。如果15分钟后没有反应,则认为测试为阴性,然后将下一种浓度添加到右眼。充血、化脓、溢血、瘙痒、打喷嚏和鼻塞的症状如前所述进行评分[18](0 =不存在;1 =轻度;2 =中度;3 =严重)。当症状评分达到5分时停止测试。结果表示为估计浓度达到五分。
体外试验
特定的IgE对天然胶乳(k82)和重组过敏原(rHev b1, rHev b3, rHev b5, rHev b6,01;采用基于荧光固相酶免疫分析(CAP-FEIA)的标准体系检测rHev b8®, Phadia,瑞典)。
嗜碱性粒细胞激活试验BAT:表示CD63作为激活标记后的嗜碱性粒细胞的百分比在体外用胶乳过敏原提取物刺激,用抗cd63 - pe和抗ige FITC单克隆抗体双标记后,用流式细胞仪检测。使用不含任何防腐剂、最终浓度为0.125和0.03125 mg蛋白质/ml (BIAL-Aristegui,毕尔巴鄂,西班牙)的无菌过滤乳胶标准水溶液提取物。
对于不同时间BAT结果的比较,后表达CD63的嗜碱性粒细胞百分比的平均值在体外用乳胶过敏原提取物在最终浓度为0.125和0.03125 mg蛋白质/ml时进行刺激。
安全
由于诱导阶段是在医院进行的,患者在治疗后30分钟内仍处于直接医疗监护下,因此直接不良事件直接记录在病例报告表中。此外,在给药前后测量心率、动脉压和峰值流量。在维护阶段,患者被指示在日记卡上注释任何不便。研究人员每次访问都监测安全性,此外,患者总是有机会联系过敏症专家或在发生严重不良反应时前往急诊室。不良反应根据欧洲过敏、哮喘和临床免疫学会(EAACI)的建议进行分类[14].
统计方法
采用平行线法分析皮肤点刺试验的皮肤反应性变化[19]及ALASA CRS PLA软件(西班牙马德里)[16].差异用皮肤耐受性指数(CTI)表示,计算方法如上所述。CTI用95%和99%置信区间表示。当CTI跨组应用时,它估计一组相对于另一组的皮肤敏感性的大小。当用于评估一组患者是否观察到变化时,CTI高于1表示皮肤反应降低。
对于手套使用测试的评价,计算每位患者症状的评分/时间的线性回归线,分别估计达到5分的时间。在类似的程序中,对于结膜挑战测试的评估,计算个体线性回归症状的得分/浓度,以单独估计达到5分所需的浓度。
组间和组内比较分别采用非参数Mann-Whitney检验和Wilcoxon检验。p < 0.05为显著性。
结果
最初纳入的28例患者中有27例完成了第一年的随访。其余受试者因与审判无关的个人原因退出。在双盲试验结束时,活跃组的1名患者和安慰剂组的4名患者拒绝参加随后的积极治疗的开放标签阶段。在第二年,又有3例患者退出,最终有19例患者完成了2年的随访1).总而言之,11例患者接受了2年的积极免疫治疗,22例患者接受了1年的积极免疫治疗(第一年14例,第二年8例)。
治疗开始前,活性组对NRL的皮肤敏感性与安慰剂组相似(CTI 2.45;95%置信区间:0.59—-13.95)。经过一年的双盲期后,接受积极免疫治疗的患者对过敏原的皮肤敏感性无明显变化(3.11;95%置信区间:0.87—-15.26)。
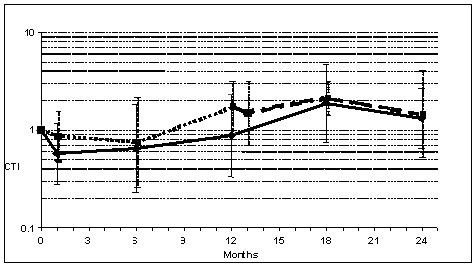
当组内CTIs(图2),将T1、T2结果与初始值(T0)进行比较,1年后活动组无差异(0.88;95%CI: 0.33-2.37)或2年积极免疫治疗(1.32;95%置信区间:0.66—-2.63)。在安慰剂组,安慰剂治疗一年后没有观察到差异(1.71;95%CI: 0.92-3.18)也没有经过2年的随访,最后接受积极免疫治疗(1.45;95%置信区间:0.52—-4.05)。当安慰剂组仅评估积极免疫治疗的年份时(T2/T1比较),也没有发现差异(0.65;95%置信区间:0.18—-2.35)。
在诊断时,除一名患者外,所有患者对至少一项挑战试验呈阳性。该患者符合纳入标准,因为在过去两年接触乳胶后出现症状。24/28例GUT阳性,26/28例CCT阳性。在随访期间,没有观察到GUT或CCT反应的改善,并且在活性组或安慰剂组中改善的患者数量与恶化的患者数量相似(表2)4).获得5个症状点(CCT-5)的CCT中nrl浓度的平均值在活跃(16.6 mg/ml;95%CI 5.8-27.3)和安慰剂(24.4 mg/ml;95%CI 4.2 ~ 44.5)组。比较T0和T1的平均CCT-5在活动期的无显著改善(T1时的平均CCT-5: 27.1 mg/ml;95% CI 5.8-48.3)和安慰剂组(T1时平均CCT-5: 35.2 mg/ml;95% ci 0-71.9)。在T1时,活性组与安慰剂组之间无统计学差异。
在获得5点症状(GUT-5)的GUT中,活跃组(23.8分钟;95%CI: 1 - 52)和安慰剂(28.6分钟;95%CI: 4.3 ~ 52.8)组。比较T0和T1的平均GUT-5仅在安慰剂组观察到改善(T1的平均GUT-5: 64.0分钟;95% ci: 0.1 - 130.4);活动组T1时GUT-5平均(18.5 min;95% CI: 8.7 - 28.3)恶化。在T1时,活性组与安慰剂组之间无统计学差异。
在28例入选受试者中,诊断时IgE-k82阳性的有27例,IgE-Hev b5阳性的有15例,IgE-Hev b6阳性的有19例。其余重组变应原(IgE-Hev b1、IgE-Hev b3、IgE-Hev b8)仅2例阳性。
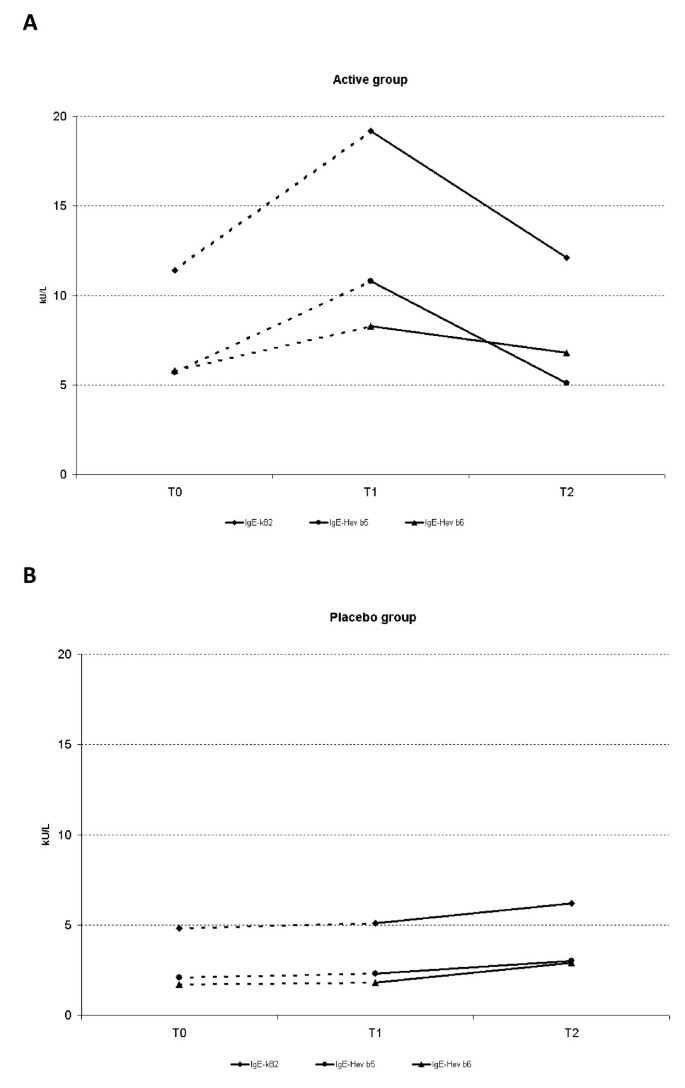
在任何研究时间(T0, T1或T2),活性组与安慰剂组相比,特异性IgE水平(k82, Hev b5, Hev b6)均未观察到变化。活跃组在整个治疗过程中观察到轻微但不显著的增加,随后下降到基线值(图3.).在安慰剂组中,第一年没有观察到变化,但与另一组相似,在积极治疗的第二年之后观察到无显著增加。
在研究开始时,活跃组中14/14的患者BAT阳性,安慰剂组中12/14的患者BAT阳性。在双盲试验结束时,分别有12/14和12/13例患者被证实为阳性,没有观察到任何变化。然而,在随访结束时,两组均有明显改善(6/11阳性受试者;4例阴性,1例不可评估)和安慰剂组(仅经过一年的积极免疫治疗,4/8例阳性,3/8例阴性,1例不可评估)。在T1时,活性组和安慰剂组在NRL浓度为0.03 mg/mL时被激活的嗜碱性粒细胞百分比的平均值之间没有观察到统计学差异(数据未显示)。
活跃组在治疗2年后,被激活的嗜碱性粒细胞的平均百分比下降,安慰剂组在积极治疗2年后也有所下降。此外,根据积极治疗的年数,BAT下降的患者比例更高(表2)5).
所有患者均达到最大剂量,无严重不良事件发生。在诱导期共记录了9例轻度不良事件,安慰剂组4例患者中有5例在安慰剂治疗的建立期间(1例结膜炎,1例鼻炎,1例瘙痒,1例呼吸困难,1例舌头瘙痒)发生在免疫治疗的第一次剂量;活性组的4名患者出现4例反应,这些反应是在达到高剂量乳胶过敏原提取物时出现的(1例舌瘙痒,3例鼻结膜炎)。只有与安慰剂组相对应的一名患者的累积计划进行了修改。
在维持期,一名患者在积极治疗一年后因前几个月皮肤瘙痒而退出治疗。另一名患者在研究的第二年从安慰剂转向积极治疗,在一周的保养后,他的脚突然出现急性皮炎,然后退出了研究。
讨论
80年代观察到的乳胶过敏发病率的增加与乳胶手套的使用增加了25倍有关,以防止传播病毒疾病(主要是艾滋病毒、BHV和CHV)发病率的增加[20.].尽管天然橡胶乳胶暴露在卫生环境中大大减少,但由于其功能特性,乳胶是制造各种产品的基础,甚至现在在其他专业人员(美发师、食品服务人员、清洁工人、警察)或人员场所,包括体育场所,仍广泛分布着含有乳胶的产品。[21].因此,由于很难完全避免过敏原,建议对那些主要有潜在职业暴露的患者进行特异性脱敏,因为预计在意外暴露的情况下,反应会比非低敏过敏患者更轻。
舌下给药可作为传统皮下免疫治疗的一种有利选择,其疗效和安全性应针对每种过敏原进行不同的验证。在这项研究中,通过适当的随机和盲法设计,对一种缺乏有效性和安全性证据的市售舌下免疫疗法进行了评估。必须强调的是,这是一个独立的临床试验,仅由公共基金建立。尽管如此,该研究是根据良好临床实践指南进行的,包括由外部研究者进行适当的监测。
随机、对照和盲法临床试验是评价新药的标准。然而,由于舌下疗法已在市场上出售,因此在伦理上不适合进行为期2年的安慰剂对照试验。因此,我们选择了一种联合设计,包括第一年的双盲安慰剂对照治疗,然后再进行一年的开放标签随访。这种设计允许对两者进行评估,在第一年比较活动组和对照组,以及评估2年内积极治疗的演变。
临床研究的一个常见困难是病人的登记。在我们的研究中,我们直接联系了所有在研究中心确诊的乳胶过敏患者,要求他们参加试验。最终评估的患者数量可以被认为是真正具有代表性的,值得注意的是,在健康区注册的NRL过敏患者总数中,超过1/3最终参与了这项研究。然而,从双盲切换到开放标签阶段的退出数量高于预期。部分原因是缺乏疗效的主观感觉,部分原因是症状出现频率低和不需要治疗的主观感觉。尽管有两名患者因皮肤症状急性复发而放弃了研究(两人都有既往特应性皮炎病史)。大多数患者在诊断前职业接触过乳胶,其中60%是卫生保健专业人员。积极组和安慰剂组的卫生保健工作者分布很平衡。除了患有哮喘的患者数量主要被分配到活动组外,人口统计学和临床特征和基线特征很好地匹配。此外,NRL特异性IgE也有差异,在活动组也更高。
在致敏原分布方面,所有患者的乳胶致敏模式一致,主要识别Hev b5和Hev b6过敏原,这两种过敏原被认为是职业性乳胶接触患者的主要过敏原[22].只有2例患者对Hev b1过敏,这是一种与脊柱裂患者和重复手术有关的过敏原。根据制造商的信息,对这些病例的个别评估显示,他们对治疗没有反应,这可能部分归因于在免疫治疗中使用的提取物的成分中不存在Hev b1。
与其他疾病相比,该研究还存在过敏临床试验的一个常见弱点,即缺乏一个单一、客观、可靠且易于测量的变量来评估治疗效果。因此,在免疫治疗研究中,疗效分析通常依赖于几个临床或分析变量、自我问卷、生活质量测量等。此外,乳胶免疫疗法的特殊情况与使用其他过敏原的临床试验相比有额外的困难,因为一些常用的变量(症状评分,药物消耗)是无用的,因为患者避免接触过敏原,因此这些参数是不可测量的。尽管其他作者[12]已经使用临床评分来评估乳胶提取物的疗效,当预期没有致敏性暴露时,使用这种评估不被认为是合适的。然而,在我们的研究中,这一困难通过使用几种方法克服了在活的有机体内(皮肤点刺试验,CCT, GUT)和在体外试验(特异性IgE和BAT的测定),以评估对免疫治疗的治疗反应。
该研究的主要结果是在研究的大多数变量中缺乏显著差异,并且在所有不同的比较中都没有进行:组之间的比较(活跃与安慰剂组在治疗一年后),以及积极治疗一或两年后的组内。
唯一具有统计学意义差异的变量是与安慰剂组相比,活性组BAT中与NRL接触而激活的嗜碱性粒细胞百分比下降。其他已发表的研究表明,在口服花生免疫治疗4个月后,被激活的嗜碱性粒细胞的百分比显著下降,分析了试验中使用的一种浓度(10 μg/ml)过敏原的结果[23].然而,这一发现的临床意义尚不清楚,因为没有明确的关系存在与其余研究变量。在未来,需要更多的研究来探索这一发现。
特异性IgE的演变仅在患者接受积极治疗时才出现最初的增加,而在积极治疗组,随后在治疗的第二年下降,与免疫治疗的短暂免疫效应一致。
令人惊讶的是,之前的一项非对照研究[11],在相似数量的患者(26例)中,仅在治疗10周后(4天的累积阶段,随后是9周的维持阶段),手套使用测试和摩擦测试就有所改善。然而,与我们的试验一样,平行线法针刺试验没有检测到变化。另一个类似的临床[12]在35名患者中使用相同的提取物,在治疗12个月后,活跃组的症状和药物评分均有所改善。这项研究设计得很好,但某些方面需要进一步澄清,因为没有提供关于患者职业和暴露于乳胶的患者数量的数据。此外,研究中发现的差异可以用两组中NRL暴露的不同来解释。鉴于nrl过敏患者在诊断时症状发生率较低,我们不再将症状和用药评分作为变量。然而,与我们的结果相反,作者在治疗12个月后确实发现安慰剂组和积极组在手套使用测试得分上有显著差异。
在治疗的累积阶段记录了低频率的不良反应,所有患者都达到了高剂量。然而,两名患者因在维持期出现皮肤症状而不得不退出研究。这些发现与最近一项涉及12例患者的试验报告大相径庭,该试验中有3例患者在诱导期因严重不良事件退出[13].然而,这一解释可以依赖于这样的事实,即2例患者有栗子过敏事件的历史,众所周知乳胶致敏与水果过敏(包括坚果)有关。
考虑到治疗的耐受性如何,疗效的缺乏可以用治疗维持阶段使用的低剂量来解释。在累积阶段,第4天达到500 mcg的剂量,但从那时起,在其余的治疗中,剂量仅为40 mcg/d。因此,可以假设在维持阶段应使用更大的剂量,特别是在希望产生长期效果时。活动组和安慰剂组之间的低样本量、NRL触发哮喘患者分布的差异以及特异性IgE对NRL的方式也可能影响疗效的缺乏。
结论
总之,需要进一步的研究来评估已测定的nrl舌下免疫疗法的疗效。具体而言,应探索在维持阶段使用更高剂量,因为积聚阶段的最大剂量已显示出良好的耐受性。然而,目前的研究对这种免疫疗法是否适用于那些可以避免接触乳胶的患者提出了一些质疑。
参考文献
坚果AF:接触荨麻疹橡胶。中华皮肤病学杂志,1997,19(5):597-8。10.1111 / j.1365-2133.1979.tb11893.x。
Forstrom L:通过乳胶手术手套接触荨麻疹。接触性皮炎。1980,6(1):33- 34。10.1111 / j.1600-0536.1980.tb03887.x。
Carrillo T, Blanco C, Quiralte J, Castillo R, Cuevas M, Rodriguez de Castro F:温室工人乳胶过敏的患病率。中华过敏临床免疫杂志,1995,16(4):489 - 497。
Rolland JM, O'Hehir RE:乳胶过敏:一种治疗模式。临床经验与过敏。2008,38(6):898-912。10.1111 / j.1365-2222.2008.02984.x。
王晓明,王晓明,王晓明:德国医护人员职业性接触性荨麻疹发病率的研究进展。中华过敏临床免疫杂志,2004,14(2):347- 351。10.1016 / j.jaci.2004.05.054。
Lavaud F, Prevost A, Cossart C, Guerin L, Bernard J, Kochman S:乳胶、鳄梨、梨和香蕉过敏:免疫印迹中30kd抗原的证据。中华过敏与临床免疫杂志,2003,22(2):357 - 357。10.1016 / s0091 - 6749(95) 70318 - 7。
Fernández de Corres L, Moneo I, Muñoz D, Bernaola G, Fernández E, Audicana M, Urrutia I:栗子和香蕉对荨麻疹患者的致敏性和乳胶接触过敏反应。中华过敏杂志,1993,70(1):35-9。
Smith AM, Amin HS, Biagini RE, Hamilton RG, Arif SA, Yeang HY, Bernstein DI:卫生保健工作者在避免使用天然橡胶乳胶后,对天然橡胶乳胶蛋白的经皮反应持续存在。临床经验与过敏反应。2007,37(9):1349-56。10.1111 / j.1365-2222.2007.02787.x。
Leynadier F, Herman D, Vervloet D, Andre C:在过敏医护人员中,标准化乳胶提取物与安慰剂的特异性免疫治疗。中华过敏临床免疫杂志,2000,16(3):585- 591。10.1067 / mai.2000.109173。
Sastre J, Fernandez-Nieto M, Rico P, Martin S, Barber D, Cuesta J, de las Heras M, Quirce S:标准化乳胶提取物对过敏工人的特异性免疫治疗:一项双盲、安慰剂对照研究。中华过敏临床免疫杂志,2003,11(5):985-94。10.1067 / mai.2003.1390。
Patriarca G, Nucera E, Pollastrini E, Roncallo C, Buonomo A, Bartolozzi F, De Pasquale T, Gasbarrini G:舌下脱敏:乳胶过敏问题的新方法。中华麻醉学杂志,2002,26(4):359 - 359。目录
Cistero Bahima A, Sastre J, Enrique E, Fernandez M, Alonso R, Quirce S, Gandarias B, Parmiani S, Rico P:乳胶提取物舌下rush免疫疗法的耐受性及其对皮肤乳胶反应性的影响。过敏临床免疫杂志,2004,14(1):17-25。
Nettis E, Colanardi MC, Soccio AL, Marcandrea M, Pinto L, Ferrannini A, Tursi A, Vacca:乳胶性荨麻疹患者舌下免疫治疗的双盲安慰剂对照研究:一项为期12个月的研究。中华皮肤病学杂志,2007,26(4):344 - 344。10.1111 / j.1365-2133.2006.07738.x。
Buyukozturk S, gelinck A, Özseker F, Çolakoglu B, Dal M:乳胶舌下免疫治疗:其安全性能否预测。中华过敏与哮喘杂志,2010,34(4):339-342。10.1016 / j.anai.2010.01.014。
Malling H,周B:立场文件:免疫治疗。过敏反应。1993,48(14增刊):9-35。
Martin S, Cuesta P, Rico P, Cortes C:基于平行线分析皮肤试验的计算机程序。中国生物医学工程学报,1997,33(1):377 - 377。10.1111 / j.1398-9995.1997.tb02552.x。
Hamilton RG, Adkinson NF:乳胶过敏受试者乳胶手套刺激程序的验证。中华过敏与哮喘杂志,1997,19(3):366 - 366。10.1016 / s1081 - 1206 (10) 63013 - x。
Abelson MB, Chambers WA, Smith LM:结膜过敏原挑战。研究过敏性结膜炎的临床方法。中国眼科杂志,2000,20(1):1 -8。
Finney DJ:生物分析中的统计方法。牛津大学学报,1979,3
控制CoD:卫生保健机构中预防艾滋病毒传播的建议。Morb Mortal Wkly代表1987,3-18。增刊2
Untersmayr E, Lukschal A, Hemmer W, Harwanegg C, Breiteneder H, Jarisch R, Scheiner O, Jensen-Jarolim E:乳胶运动带对乳胶过敏患者有风险。中国生物医学工程学报,2008,29(4):344 - 344。10.1016 / j.imlet.2007.10.008。
Wagner S, Breiteneder H:橡胶树乳胶过敏原:当前面板和临床相关性。中国免疫过敏杂志,2005,36(1):357 - 357。10.1159 / 000082938。
Jones SM, Pons L, Roberts JL, Scurlock AM, Perry TT, Kulis M, Shreffler WG, Steele P, Henry KA, Adair M, Francis JM, Durham S, Vickery BP, Zhong X, Burks AW:花生口服免疫治疗的临床疗效及免疫调节。中华过敏临床免疫杂志,2009,29(2):332 - 332。10.1016 / j.jaci.2009.05.022。
确认
该研究的部分资金由FIS (PI04/2301), Fundación SEAIC 2004, Fundación Jesús Gangoiti Barrera 2004提供。
作者感谢Pilar Rico和Santiago Martin(西班牙ALK-Abello医学系)在皮肤点刺试验的评估和统计分析方面的合作。
作者信息
作者及隶属关系
相应的作者
额外的信息
相互竞争的利益
作者宣称他们之间没有利益冲突。
作者的贡献
GG参与了研究设计、患者入组、统计分析和手稿起草。JA参与了研究设计、统计分析和文稿起草。OU参与了患者的入组、统计分析和稿件的起草。MTA参与了患者的招募和手稿的起草。EF参与了患者注册。MLS进行了免疫测定。DM参与了患者的招募和手稿的起草。所有作者都阅读并批准了最终的手稿。
权利和权限
本文由BioMed Central Ltd授权发布。这是一篇开放获取文章,根据创作共用属性许可协议(http://creativecommons.org/licenses/by/2.0),允许在任何媒介上不受限制地使用、传播和复制,前提是正确地引用原始作品。
关于本文
引用本文
加斯达明扎,G.,阿尔戈塔,J.,乌列尔,O.。et al。舌下免疫治疗天然胶乳过敏患者的随机、双盲、安慰剂对照临床试验。试用12, 191(2011)。https://doi.org/10.1186/1745-6215-12-191
收到了:
接受:
发表:
DOI:https://doi.org/10.1186/1745-6215-12-191
关键字
- 安慰剂组
- 皮肤点刺试验
- 维护阶段
- 天然胶乳
- 过敏原提取物