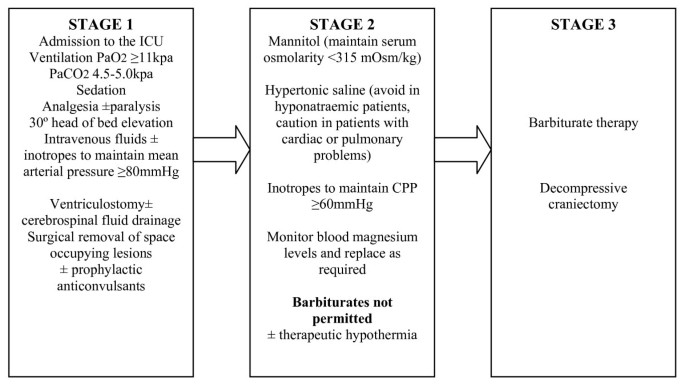
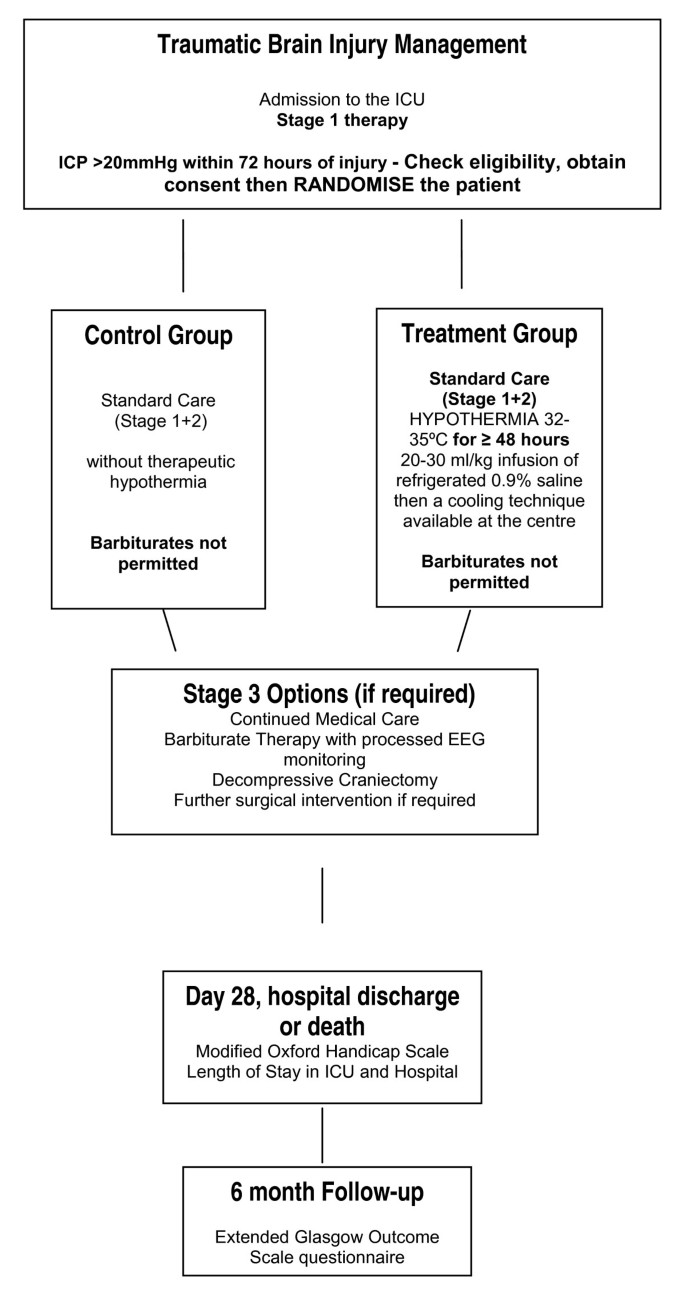
这是一项实用的、多中心随机对照试验,旨在检查低温(32-35°C)对创伤性脑损伤后结局的影响。这项研究为期41个月。参与者被随机分为对照组或干预组(图2).分配到对照组的参与者接受标准治疗,没有治疗性体温过低。随机分配到干预组的参与者接受标准的治疗性低温治疗。通过静脉注射20- 30ml /kg冷冻0.9%生理盐水开始低体温,并使用该中心可用的冷却技术维持。在干预组中设计了诱导和维持治疗性低体温的流程图。体温过低的深度(范围:32-35°C)由ICP指导,较高的压力水平保证较低的目标温度。在干预组中,已经制定了检测和治疗颤抖的指导方针。这是专门为这次试验设计的,借鉴了:
治疗组维持32-35°C的治疗性低体温至少48小时。先前的研究表明,持续至少48小时的治疗性低温有降低TBI后死亡率和改善神经功能的趋势[42].持续低体温至必要时,以降低并维持ICP <20 mmHg。脑外伤基金会指南将颅内压定义为>20 mmHg [37].在治疗性低体温的同时,干预组的所有患者继续接受1期和2期治疗,以降低颅内高压[37,38].如果升高的颅内压对这些治疗产生耐药性,尽管降低体温的深度增加,治疗可能会升级到包括3期干预。如果需要,应终止分配到治疗组的患者的治疗性低体温治疗,并使用再温指南重新加热患者。治疗升级的原因应记录在每日数据收集表上。
Eurotherm3235Trial的主要终点是TBI后6个月使用GOSE问卷的结果。在协调中心随机分配参与者6个月后,通过邮寄方式向参与者发送GOSE问卷和求职信。
研究人群
样本大小
共纳入1800例患者(每治疗组900例)。全世界至少将启动70家专门护理创伤性脑损伤患者的医院,包括比利时、德国、意大利、荷兰、西班牙、瑞典和英国的中心。
入选标准
- 1)
据信同意参加研究的法定年龄是65岁
- 2)
原发性闭合性脑外伤
- 3)
一线治疗后ICP升高> 20mmhg≥5分钟,无明显可逆性原因,如患者体位、咳嗽、镇静不足
- 4)
头部受伤后≤72小时
- 5)
冷却装置或技术可用于>48小时
- 6)
核心温度≥36°C(随机分组时)
- 7)
脑部CT扫描异常。这被定义为有血肿、挫伤、肿胀、疝出或基底池受压。
排除标准
- 1)
病人已经接受了低体温治疗
- 2)
随机分组前给予巴比妥酸盐输注
- 3)
重症监护室会诊医师或神经外科会诊医师认为患者不太可能存活24小时
- 4)
入院时温度≤34℃
- 5)
妊娠(所有符合纳入标准的育龄女性患者将进行尿妊娠试验。这是由ICU的研究者或研究护士进行资格筛选程序的一部分)。
参加者选择及报名
确定参与者
符合条件的参与者由ICU的护理和医务人员确定。
自愿参与者
符合本研究条件的患者必须有颅内压升高,尽管头部损伤的治疗方案为1期。第1阶段治疗方案包括镇静和通气,因此参与者自己不能给予知情同意。
患者和亲属信息表是在与遭受创伤性脑损伤的患者及其亲属协商后设计的。咨询是在爱丁堡Headway集团的收容中心进行的,这是一个为脑损伤患者注册的慈善机构http://www.edinburghheadway.org.uk.
资格甄别
所有符合条件的患者都要完成筛查记录。本表格收集符合纳入标准、不符合排除标准以及获得同意的日期等数据。它被锁在中心的一个柜子里。这些数据通过电子病例报告表(CRF)输入试验数据库,以便试验办公室监测每个站点的招聘和/或拒签率。
随机
患者在符合纳入标准后应尽快随机分组。根据每个站点的可用技术,使用基于中央互联网的随机化服务或电话随机化服务对参与者进行低体温或标准护理的随机化。
使用以下基线协变量最小化治疗分配(但包括随机元素以确保分配隐藏):
- 1)
试验中心
- 2)
年龄<或≥45岁
- 3)
复苏后格拉斯哥昏迷评分运动部分1-2或3-6
- 4)
受伤时间<或≥12小时
- 5)
瞳孔:都有反应或只有一个或没有反应
治疗分配
不可能对当地调查人员的分配情况视而不见,因为在临床上,哪些患者正在接受低温治疗是很明显的,例如所需的设备、患者体温、血液结果、液体需求。然而,由于GOSE问卷由协调中心分发给参与者,因此确保了结果数据评估的盲化。
过早退出
参与任何研究试验都是自愿的,因此参与者或其法定代表人可以在任何时候退出试验。如果是这种情况,应在提前退出表上明确说明以前收集的数据是否仍可用于分析,以及患者将从试验的哪一部分退出:
1)完全退出-安全终止低体温干预,不再收集进一步的数据,以前收集的数据将不会用于分析。
2)完全退出-不收集进一步的数据,干预安全终止,但以前收集的数据可以用于分析。
3)退出干预,但愿意接受随访。
4)只接受随访。
如果患者希望退出试验或其法定代理人希望退出试验,他们可以自由地这样做,无需说明理由,患者的医疗护理或合法权利也不会受到影响[47].然而,如果患者因医疗原因被负责其护理的医生退出研究,则必须在数据收集表中清楚地记录退出的原因,并在适当时填写一份严重不良事件表。
数据收集与检查
所有患者的每日数据收集从随机化(基线)当天开始,一直持续到ICP监测仪被移除为止。使用电子CRF收集数据。这包括在出院时完成的改良牛津障碍量表。所有crf的纸质副本都可提供给很少或没有互联网接入的中心。所有crf必须用英语完成,并由Lincoln, Paris管理。盲法数据和患者身份数据分别存储在安全数据库中。所有患者身份数据都由协调中心存储。
随访数据
患者的全科医生/家庭医生会收到一封邮件,告知他们患者参与了eurotherm3235试验。
损伤后6个月,使用GOSE问卷评估患者预后。由于这是研究的主要终点,因此获得这一信息至关重要。如果患者在受伤后6个月仍在医院,研究护士或调查员可以在适当的情况下到病房看望患者,与他们一起进行问卷调查。然而,如果患者已经出院,问卷将被发送到他们的居住地址。在向患者发送问卷之前,试验小组的一名成员将打电话给患者的家庭医生,了解他们的生命状况。
由于受伤的性质,患者很可能无法自行完成问卷。因此,我们也会向同意患者的人发送一封信,邀请他们帮助患者完成表格,并提醒他们这项研究。这与GOSE问卷发送给患者的同时发送。如果在3周内没有收到患者的回复,他们会收到一份简短的GOS问卷和一封求职信。
如果仍然没有回应,病人已经出院,将尝试通过电话直接与他们联系。如果患者在出院时缺乏能力,且无法通过电话直接联系到患者,则会打电话给同意将患者纳入研究的人,并要求他通过电话填写更短的GOS问卷。
然而,如果患者在出院前恢复了能力,并同意继续参与研究的随访阶段,但无法通过电话直接联系,则不再进行进一步联系。这个过程在同意程序中讨论。
爱丁堡的工作人员与当地调查人员密切合作,以获得尽可能完整和准确的数据。关键数据,如结局指标,100%重复输入试验数据库。广泛的范围和一致性检查进一步提高了数据的质量。
统计与数据分析
样本量计算
该试验的主要终点是通过GOSE问卷测量的6个月的结果。2000年至2008年间发表的六项荟萃分析收集了治疗性体温过低的主要证据。其中包括不同数量的临床试验,并根据随机化和盲法程序的质量评估对每个试验进行检查。所有荟萃分析均发现低温对神经系统预后有积极影响的趋势,但只有两项研究达到统计学显著性[37,38].
先前TBI III期试验失败的一个主要原因是,它们通常检测到不良结果的绝对下降约10%。鉴于外伤性脑损伤人群的巨大异质性,这是一个不切实际的目标。较为温和的7%的绝对下降仍然具有临床相关性,并且作为一种假设的治疗效果更为现实(对应于0.75的优势比)。815组的两组在5%显著性水平(双侧)下给出80%的功率来检测不良结果从60%下降到53%,900组的两组在相同显著性水平下给出83%的功率来检测相同的差异。我们的目标是在主要试验中招募1800名患者,以便对损失进行随访。重要的是,我们一直对能量计算持保守态度,以减少在该领域进行另一次能量不足试验的机会。
建议的初步分析
在锁定试验数据库进行分析之前,将最终确定详细的统计分析计划(SAP),列出拟议分析的全部细节。初步分析将遵循以下原则:
分析将根据“意向治疗”原则进行。
估计的治疗效果将连同其相应的95%置信区间。
对主要结果测量(6个月GOSE)的分析将利用结果量表的序数性质。目前,在脑外伤和中风试验方法学中,一个活跃的研究问题是使用哪种方法来分析这种顺序结果量表,两种主要选择是“移位分析”和“滑动二分法”。考虑到目前正在进行的方法学研究的结果,将在SAP中宣布首选方法。
主要分析将根据关键基线协变量进行调整,将在SAP中指定。未调整的分析也将作为敏感性分析进行展示。
由独立的数据和安全监测委员会审查的所有中期疗效分析将根据严格的Peto-Haybittle指南进行解释,因此不需要调整最终p值以进行多次试验。
其他计划分析
先天的亚组分析将测试最小化因素之间的关系,包括:年龄<45岁,入院后复苏格拉斯哥昏迷评分运动反应<2,受伤时间<12小时和结局。分析将测试相互作用的影响,并将寻求更严格的统计显著性水平(p < 0.01),以反映这些亚组分析的探索性。在这些分析中只使用主要的结果测量。
一些中心将进行其他探索性和观察性研究。这些子研究将由当地研究人员进行,并需要试验管理和指导委员会的批准以及进一步的伦理批准。所有子研究也必须获得外部资助。
经济分析
经济数据的收集和分析工作将依赖于获得外部资金。该分析的细节将在获得外部资金时补充。
不良事件
的只有需要收集的严重不良事件包括:
试验管理和监督安排
项目管理小组
试验将由一个项目管理小组进行协调,该小组由资助人和爱丁堡的首席研究员、试验经理和顾问组成。
审判管理
试验办公室与爱丁堡大学的爱丁堡临床试验单位相关联,并为临床中心提供日常支持。审判办公室工作人员负责审判管理的各个方面。这些职责包括向所有中心提供研究建议和支持,确保与所有中心合作及时完成crf,进行数据检查和分析。试验办公室的工作人员还负责为资助该研究的数据和安全监测委员会(DSMC)、试验指导委员会(TSC)、伦理委员会和欧洲重症监护医学学会(ESICM)制作进度报告。研究结果的出版和传播将由爱丁堡临床试验部门与首席研究员和主要研究员合作协调。
高级试验经理负责监督研究,并向首席研究员负责。两名试验经理负责监督试验的日常工作,包括:启动试验中心,确保培训记录的保存和更新,监督和支持所有试验工作人员,对所有参与试验的中心进行实地考察,定期与所有试验调查员联系,监测试验中心和试验场的关闭情况。秘书/数据文员负责试验的所有行政职责,包括:从纸质crf中手动输入数据,监测后续问卷的响应,与当地调查人员一起跟进缺失数据查询和未回复问卷的情况。
主要临床试验的统计和科学完整性通过纳入三个不同的统计学家角色来增强:研究统计学家,承担所有统计任务,包括正式分析和数据报告,DSMC和独立统计学家。该统计员是真正独立的,除了在指定的时间为DSMC制作无盲中期报告外,不参与任何试验。
在获得额外经费的情况下,卫生经济学家负责编制经济评价所需的数据收集表格,分析经济数据并编写最后报告的经济评价部分。
一名资讯科技程式设计师已建立资料库管理系统,以有效地进行试验,包括随机分组、及时发放问卷、自动监察表格、数据验证及清理。
试验督导委员会
TSC负责监督审判的进行和进展。应指导委员会主席的邀请,试验管理小组的其他成员可作为观察员出席。
数据和安全监测委员会
已经成立了一个独立的DSMC来监督试验参与者的安全。在招募试验人员期间,中期分析将在严格保密的情况下,连同委员会可能要求的任何其他分析一起提供给DSMC。
根据这些分析,如果委员会认为试验中的随机比较提供了以下任何一项,DSMC将通知TSC:
- 一)
对于所有或某些类型的患者,明确表明干预措施的证据,排除合理怀疑。(或禁忌症)在各组发病率和死亡率的净减少方面。(排除合理怀疑的适当证明标准无法精确规定。在主要终点的中期分析中,至少有三个标准差的差异可能需要证明过早停止或修改这样的研究。如果采用这一标准,它将具有实际的优势,即中期分析的确切数量将不太重要,因此没有提出固定的时间表(Peto R et alBr J癌1976;34: 584 - 612)。
- b)
了解本试验和可比试验结果的临床医生可以合理地预期,这些证据将对需要在ICU进行ICP管理的患者的护理产生实质性影响。
- c)
注册无效。
然后TSC将决定是否修改招募试验。除非发生这种情况,否则TSC、项目管理小组、临床合作者和试验办公室工作人员将继续对中期结果一无所知。DSMC的运作是根据达摩克利斯原则[48].
查阅记录
主要研究人员和参与研究的机构将允许试验相关的监测、审计、研究伦理委员会审查和监管检查。在审核的情况下,研究者同意允许主办方、主办方代表或监管机构直接访问所有研究记录和源文件。
研究监测
试验管理人员将代表共同发起人对该研究进行监测。现场工作人员应便于监测访问,并必须确保所有所需文件可供审查。
在招募开始前,研究启动访问将在所有地点进行。在整个试验期间,在招募超过10名患者的地点进行现场监测。在这些监测访问期间,试验经理对试验数据进行源数据验证,对知情同意书进行验证,并确保研究者现场档案的完整性。对于招募少量患者的场所不进行常规监测。但是,试验数据的中央质量控制检查将按照第6.0节所述进行。如果数据的中央质量控制发现任何试验场的数据收集存在问题,或者如果首席研究员和/或联合赞助人对任何试验场的试验数据的质量或有效性存在担忧,将进行现场监测访问。
通过试验监测发现的研究方案和/或良好临床规范的严重违规行为将立即通知联合主办方,并采取适当的纠正措施并记录在案。