研究目的
外科医生进行的VS VS与介入放射科医生进行的VS。
所需患者人数
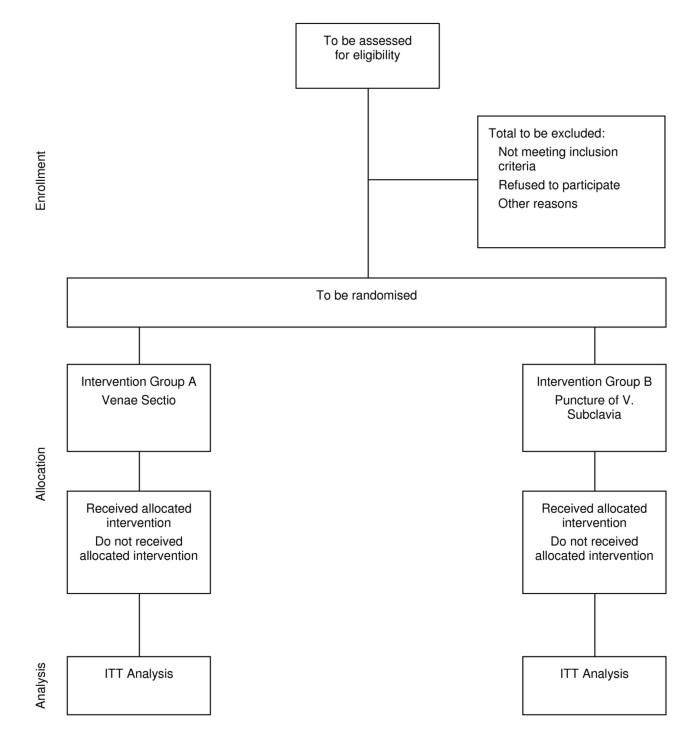
一项已发表的文献综述显示,在回顾性和前瞻性研究中,VS的初次成功率中位数为80% [1,2,9- - - - - -15].在多项回顾性研究中,PVS的主要成功率中位数为99% [3.- - - - - -8].采用简单交互统计分析(SISA)计算双侧检验的组数[16].如果成功率差异为19% (80% vs. 99%),则涉及100例患者(每组50例)的试验有80%的几率在5%的alpha水平上检测到显著差异(图1).我们决定根据先前研究的结果计算样本量,而不是根据定义的最小临床重要差异计算样本量,因为所有提到的先前研究均显示一致的中位数差异为19%。这为在经济样本量的随机对照试验中首次检验这些结果提供了机会。
资格
入选标准
排除标准
参与另一项干预试验,干预干预和本研究的结果
缺乏依从性(由试验研究者评估)
精神状态受损或语言问题(患者无法阅读德语)
已知对造影剂过敏的患者
受试者退出标准
本人请求或者法定代表人请求
如果在研究者看来,继续试验对受试者的健康有害
所有退出的患者将在最终结果中报告,以保证最大程度的透明度。
同意
被分配在海德堡大学医院放射科或外科进行端口导管系统植入的患者,将在治疗前的访问期间对其资格进行筛选,并告知PORTAS 2试验。在要求患者知情同意之前,将详细阐明研究程序、风险、益处和数据管理。在纳入患者的个人资料(身高(cm)、体重(kg)、性别、吸烟习惯、Karnowsky-Index(0 - 100%)、免疫抑制药物、抗生素(是/否)、化疗(是/否))将被记录到CRF中(表2)1).
最小化偏差的随机化和程序
减少偏见
为了实现已知和未知风险因素的可比性组,随机分组将按1:1的分配比例按随机分组大小进行非分层分组随机化。由随机化软件RITA对治疗组进行分配®[17].根据样本量计算,将招募110例患者。随机分组将由临床研究中心外科(KSC)专业的研究护士执行,a组患者的外科和b组患者的放射科将在患者签署知情同意后进行随机分组。干预将安排在纳入后的1-4天,取决于尽可能早的手术预约。
尽量减少治疗偏差
所有参与该试验的医生将每3个月接受一次培训和更新,以确保患者获得同等的治疗。在操作和放射线室将使用专门的手册,以减少错误。所有患者都将植入相同的TIAP设备(INTRAPORT II Keramic®费森尤斯·卡比著)。抗生素预防仅适用于有心内膜炎风险的患者,或植入术后5天内化疗的患者。
尽量减少测量偏差
研究护士将记录并监督手术室或放射干预室的程序。由于手术的性质和不同部门的分配,盲手术是不可能的。
研究治疗
所有患者将以5度反向Trendelenburg位放置在手术台上。患者的颈部、胸部和肩部将被准备好,并以惯常的无菌方式覆盖。
左V. Subclavia/V.;除下列情况之一外,应优先采用头卡:
患者左侧患有乳腺癌
病人是左撇子
先前有证据表明左锁骨下静脉因血栓形成而闭合
病人的希望
患者之前左侧有导尿管
根据分配情况,程序将继续进行:
干预组A(外科医生进行静脉切开术)
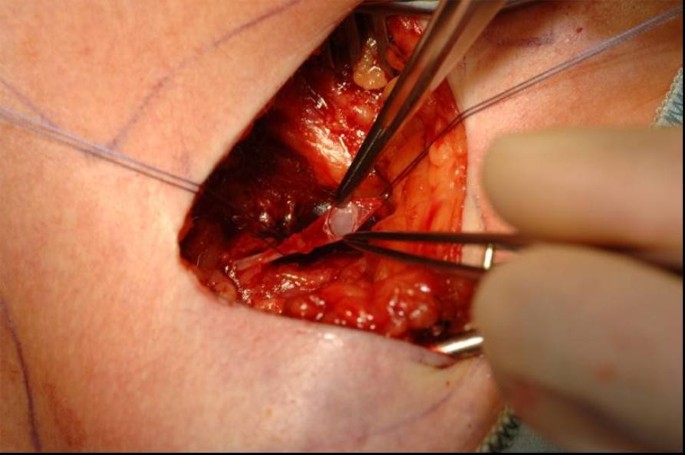
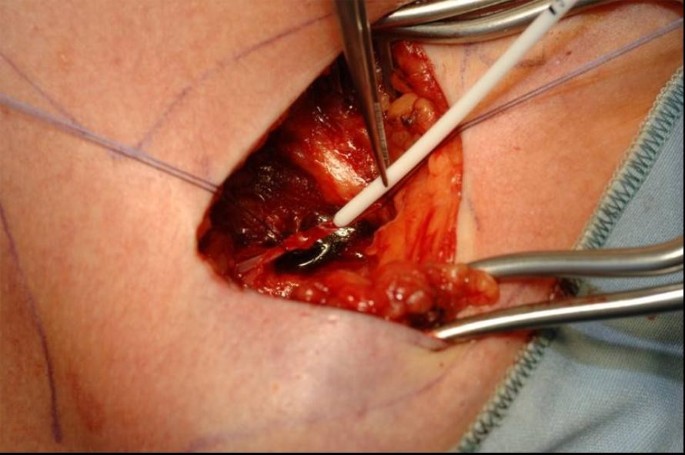
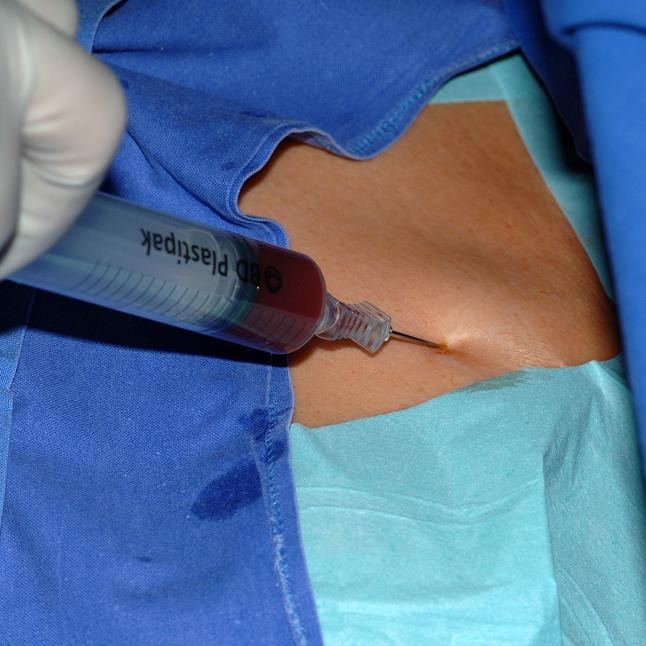
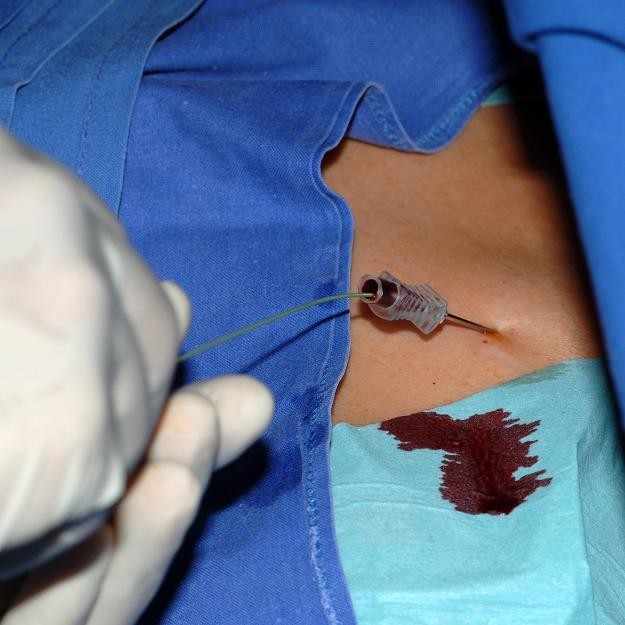
以无菌方式将局部麻醉渗透到皮肤和皮下层,并在三角胸沟区域下外侧4cm处进行皮肤切口。头静脉要露出来。头静脉远端结扎,并用可吸收缝合线绕颅。静脉将横切腹侧,导管用肝素化生理盐水冲洗,然后引入(图2,3.).导管引入时可使用导丝、静脉扩张器,必要时可使用剥离鞘。放置导管后,通过透视控制导管的正确位置(导管顶端位于上腔静脉,刚好与支气管分叉对齐)。导管将连接到端口室。使用相同的切口,将在胸筋膜上准备一个皮下袋。左腔将用三根不可吸收的缝合线固定在胸肌筋膜上。伤口将用可吸收的皮下缝线缝合,皮肤将用不可吸收的皮内缝线缝合。经皮肤穿刺(胡贝尔针)检查,血流通畅,可抽血输注。为了完成该过程,用2-4 ml肝素化生理盐水(100 I.E./ml)阻塞系统。
干预组B (V.锁骨下穿刺,放射科医生)
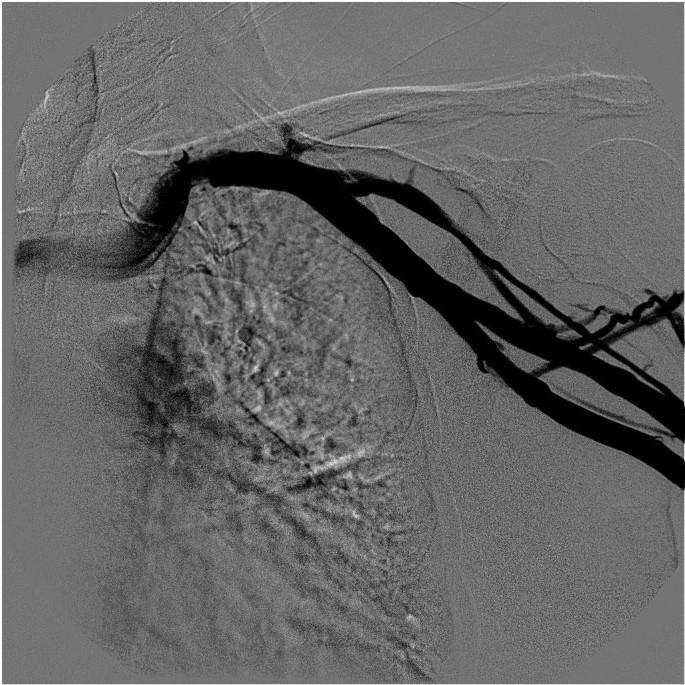
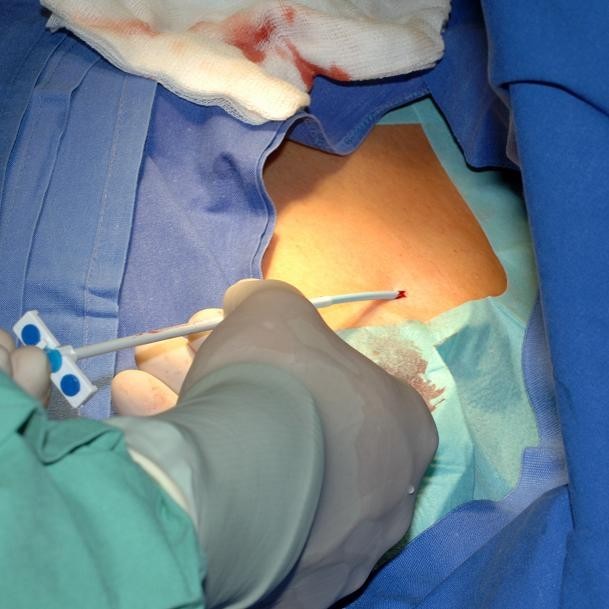
患者在计划穿刺位置一侧接受外周静脉导管,用于注射造影剂(紫外线®拜耳370)和锁骨下静脉未因血栓形成而闭合的验证(路线图技术,图4).以无菌方式将局部麻醉引入皮肤和锁骨骨膜。穿刺位置将标记在锁骨近端和内侧三分之一之间(图5).穿刺位置上方切开约2厘米宽的皮肤切口。在下文中,V.在透视下使用Seldinger技术穿刺锁骨下,并引入导丝(图6,7).引入器护套通过导丝进入V.下锁骨。所述导丝被移除,所述端口导管可通过引入器鞘引入。透视确认正确位置。在与锁骨平行的第一个切口下方1厘米处进行第二个约3.5厘米宽的皮肤切口。在胸筋膜上准备一个皮下袋。左腔将用三根不可吸收的缝合线固定在胸肌筋膜上。伤口将用可吸收的皮下缝线缝合,皮肤将用不可吸收的皮内缝线缝合。再次透视检查导管端口的正确位置(导管顶端位于上腔静脉,正好对准支气管分叉)。通过皮肤穿刺(胡贝尔针)检测抽血和输液的流量。 To complete the procedure the system is blocked with 2–4 ml heparinized saline (100 I.E./ml).
主要和次要终点
主要终点
主要终点将是随机植入技术的成功率。
主要终点的定义
初次成功定义为导管在V. Cephalica/V中的正确位置。术中通过x线片控制预期侧锁骨下,并通过抽血输液验证功能正确。
主要终点评估
术后主要成功将由负责的医生在病例报告文件(CRF)中进行评估,并由独立的研究护士确认,并将与手术报告进行比较。显示导管正确位置的术中x光片副本将保存在数字放射图像查看器软件Centricity中®-海德堡大学医院常规使用。
二次端点
围手术期并发症
气胸
hematothorax
术中神经损伤
导管或左室脱位
造影剂不耐受
术后并发症
血栓形成
术后出血
血肿
导管断开或断裂
注射液体外渗
伤口感染
皮肤坏死
定义见表2和表3.
评估
- 1.
由一名独立研究护士在手术当天用勾框记录端口植入的围手术期并发症。
- 2.
在手术当天,由研究护士进行标准化电话采访后,在随访1(手术后90天)用勾框记录端口植入术后并发症。如果患者报告有任何异常,将要求负责的家庭医生进行确认。
移植手术时间
从第一个皮肤切口到最后一个皮内缝合结的时间
从病人进入干预室到病人离开干预室的时间
评估
手术当天由一名独立研究护士在CRF中记录这两次手术。
辐射剂量
定义:剂量率与辐射面之积(Gy × cm2).
评估
该值将由研究护士从使用过的放射检查设备的显示器中复制,并记录在CRF中。
安全方面
安全变量规范
外科医生培训
对于迄今为止操作过25个或以下端口的外科医生/放射科医生和导师(高级外科医生/放射科医生),将在CRF中注明操作端口的确切数量。外科医生和导师(高级外科医生)到目前为止进行了超过25个端口手术将被分为以下类别之一:26-30个;31-35;36-40;41-45;46-50;> 50个操作端口,并记录在CRF中。
伴随药物
伴随的药物治疗将不会被记录,因为两种植入技术的主要成功率是局部和技术终点。因此,与患者药物的全身药理相互作用将是非常不可能的。
既往病史
CRF将记录患者既往和伴随的疾病。原发疾病类别(导管植入原因)是基线可比性分析的变量之一。
不良事件和严重不良事件
在研究过程中,将定期向首席研究员报告不良事件。化疗预期的症状和恶性疾病的进展不会被记录为不良事件,因为它们不太可能与手术植入技术有关。
符合次要终点定义之一的突发事件根据其记录被视为突发事件,但不必在24小时内报告给主办方(海德堡大学医院)和首席研究员(MW博士Büchler,海德堡大学医院普通、内脏和移植外科主任)。在整个研究过程中,将定期向首席研究员报告。外科和放射学试验协调员还将交叉检查所有患者的sae /AEs。
分析
对于所有接受TIAP植入手术的随机患者,将比较两个干预组的主要终点。患者将被随机分析。这符合意向治疗原则[18].此外,还将执行每个协议的分析。
主要终点的结局指标将采用连续性校正的卡方检验进行显著性检验。如果一个或多个预期细胞计数小于5,则使用Fisher的精确测试。不使用分层。初步成功的估计优势比将与95%的置信区间一起显示。二次分析将采用多元回归模型,包括治疗组、年龄、体重指数、外科医生经验和Karnofsky指数作为预测因素。除治疗组外,所有预测因子均用作连续变量。
在所有的初次成功分析中,如果患者的初次成功信息缺失,将被视为失败,但在一次敏感性分析中,这些患者将被排除在外。
所有统计分析都将使用SAS进行®软件,版本9.1(或更高)的SAS系统Unix (SAS研究所公司,卡里,NC,美国)。
研究组织
所有预定在海德堡大学医院外科或放射科门诊部进行TIAP系统植入手术的患者,将由临床研究中心外科(KSC)的成员转诊和筛选。筛选结果将记录在筛选日志中。
每年约有700名患者在海德堡大学外科和放射科门诊部接受TIAP系统植入。随机抽取110例患者的估计时间约为6个月。
PORTAS 2试验的发起人是海德堡大学医院。
独立的数据管理和统计分析将由海德堡大学医学生物计量学和信息学研究所(IMBI)根据预先指定的统计分析计划进行。
在与临床研究小组组长和生物统计学家协商后,首席研究员有权随时终止试验并从试验中心移走所有试验材料。可能要求终止试验的原因包括:
金融支持
该试验将由费森尤斯卡比股份有限公司以同等份额赞助©以及海德堡大学普通、内脏和移植外科临床研究中心(KSC)的常规研究预算(Baden-Württenberg国家)。