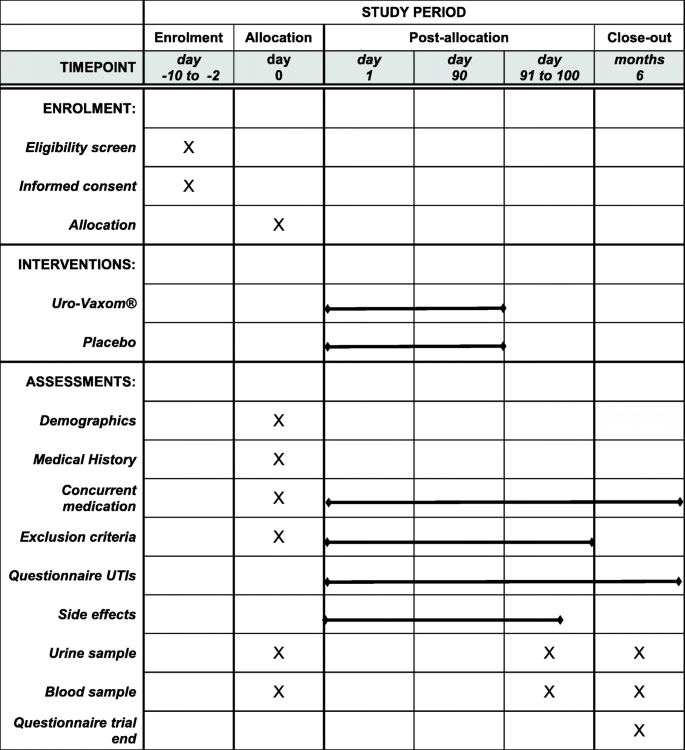
评估和收集成果的计划
可行性的结果
将保留所有筛查患者的电子列表(Microsoft Excel 2016),并收集有关资格、排除标准和登记的信息。此外,在入学前将完成关于所有纳入和排除标准的CRF文件(p)。在干预期间以及干预和随访期结束时,排除标准也将每两周记录在pCRF上。任何过早终止试验及其原因将记录在试验数据库的电子CRF中。此外,服用试验药物(胶囊/片剂)的数量将记录在eCRF中。
临床结果
在干预期间,试验参与者将每2周完成一份自行编写的关于UTI症状和治疗副作用的纸质问卷。泌尿道感染的症状如下:发烧/发抖;新的或增加的尿失禁/漏,增加的紧迫性,导尿频率增加;增加痉挛状态;萎靡不振,感觉不舒服,疲劳;尿液浑浊、恶臭;腹部/下背部/肾脏疼痛,排尿时疼痛;起鸡皮疙瘩,出汗增多。参与者可以列出所经历的任何其他症状。如果报告了至少一种膀胱症状(新的或增加的尿失禁/漏,尿急增加,导尿频率增加,排尿疼痛)和另一种症状,并伴有阳性尿液分析结果(白细胞,亚硝酸盐)和尿培养中增长≥10,000 cfu/ml(样本由医生收集),则算作有症状性UTI通过哲学的).
列出了以下副作用:头痛、腹痛、恶心、呕吐、腹泻和胃灼热。参与者可以列出所经历的其他副作用。如果出现症状性尿路感染,将从电子病历文件中收集临床常规评估数据(即尿状态和尿培养结果)和所选择的治疗方法,并记录在eCRF中。
在随访期间,试验参与者将自行编写一份关于UTI症状的纸质问卷(同上),评估(浸棒和尿培养),并每两周进行一次治疗。如果仍在住院的试验参与者出现症状性尿路感染,将从电子病历文件中收集临床常规评估(即尿状态和尿培养结果)和所选择的治疗方法的数据,并记录在eCRF中。
生物的结果
在三个评估时间点(基线、治疗结束、试验结束)采集尿液(30ml)和血液样本(30ml)。泌尿状态,蛋白质组和转录组,微生物组,标准血细胞计数和白细胞差异将被评估。
为了评估尿液微生物群,将使用Price等人描述的流线型增强定量尿培养方法培养尿液。[18].微生物鉴定将使用基质辅助激光解吸/电离飞行时间质谱(MALDI-TOF MS;Bruker Daltonics, Billerica, MA, USA)不同的殖民地。菌落形态将被描述和量化。此外,在收集后4h内,尿液将以3000rpm的速度旋转,所得的颗粒将悬浮在1ml尿液中,在−80°C下储存,直到提取脱氧核糖核酸(DNA)。DNA提取将根据制造商的协议使用QIAamp PowerFecal DNA试剂盒(QIAGEN, Hilden, Germany)完成。将使用MinION纳米孔测序仪(Oxford nanopore Technologies, Oxford, UK)进行全基因组(提取足够数量的基因组DNA)或16S测序(提取较少数量的DNA)。测序文库将使用Nanopore连接测序试剂盒(Oxford Nanopore, Oxford, UK)制备,并使用高精度模型与MinION流池进行测序。生物信息学分析将使用FASTQ WIMP(“What 's In My Pot”)(Oxford Nanopore, Oxford, UK)分析工作流,用于微生物组分析。
为了评估尿液蛋白质组和转录组的相关蛋白质,我们将使用两种样本类型:(1)离心和无菌过滤(0.22μm)尿液和(2)尿液颗粒(如果存在)。这些样品将通过酶联免疫吸附试验(ELISA)分析IgA抗体的总数量和IgA抗体的数量大肠杆菌包含在urovaxom®裂解液。使用ELISA和提取的核糖核酸(RNA)逆转录聚合酶链反应(RT-PCR)阵列测定促炎和抗炎细胞因子的数量,如干扰素(IFN)-γ、肿瘤坏死因子(TNF)-α、肿瘤生长因子(TGF)-β、白细胞介素(IL)-1β、IL-2、IL-4、IL-5、IL-6、IL-8、IL-10、IL-13。
其他感兴趣的结果
将从电子病历文件中收集患者特征、膀胱排空方法和同时用药,并记录在eCRF中。有关病史的数据将使用pCRF收集。在随访期结束时,参与者将填写一份关于他们的经验、治疗满意度和关于治疗分配的假设的自研pCRF。
计划促进参与者保留和完成随访{18b}
试验参与者在治疗期间将继续住院(见合格标准)。如果试验参与者在试验结束前出院,将计划进行电话采访,以收集关于UTIs的结果测量,以防参与者不返回自我报告问卷。
在停止或偏离干预方案的参与者中,只要参与者继续参与试验,所有结果数据都将按照方案收集。在试验提前终止的情况下,如果参与者没有拒绝将健康相关数据和样本用于研究目的(一般同意),则将收集有关UTIs的临床常规数据。
数据管理{19}.
试验源数据将记录在pcrf中或直接记录在eCRFs中(见上文)。所有数据将被加密记录。pcrf的试验数据将及时转移到eCRFs。eCRFs将保持最新,以反映受试者在试验过程中的状态。eCRFs已在基于web的数据管理系统secuTrial®(iAS, Berlin, Germany)中创建。该系统托管在一个安全的内部服务器上。只有经过培训和授权的试验人员才能将数据输入电子数据库。
在发布到生产环境之前,电子试验数据库已经由数据管理员和一名研究人员进行了测试。数据输入字段的特定定义以及输入数据值的范围和一致性检查将提高数据质量。此外,还设置了监控计划(见下文),以确保输入的数据值是准确的。在数据导出到统计软件中进行分析之前,所有输入的数据将由研究人员审查和验证,并由主要研究人员签字。
从加密样本中获得的生物数据将存储在医院的安全服务器上。只有试验小组成员才能访问数据。
保密{27}
调查人员确认并维护参与者的隐私权原则,并将遵守适用的隐私法律。在科学会议上展示数据或在科学期刊上发表数据时,将保证参与者的匿名性。通过本试验获得的个人医疗信息将被视为机密,不会透露给第三方。允许授权第三方直接访问未加密的源文件,以进行监控、审计和检查。试验工作人员将根据首席研究员的授权访问试验数据。通过使用识别代码将参与者与试验数据联系起来,从而建立保密性。识别码将不包含姓名、首字母、出生日期或任何其他个人识别号码(例如,社会安全号码、患者识别号码等)。包含指定的试验识别码和最少的个人信息(即姓名、出生日期)的名单将存储在试验现场的一个上锁的柜子中。所有crf和数据收集文件将仅以试用代码标识。试验结束后,所有试验数据将存储在一个上锁的档案室,限制访问10年。
本试验/未来使用{33}的生物样本收集、实验室评估和存储计划用于遗传或分子分析
所有生物标本的处理都将使用加密样本(血液和尿液)。每个评估时间点的样本将被转移到瑞士生物银行进行处理,该银行已由瑞士生物银行平台(SBP)审核和认证。样品的处理最好由一个由两人组成的团队(最好)根据经过验证的工作流程和标准操作程序(sop)完成,从最易腐烂的样品(尿液)开始,以确保尽可能短的处理时间(从针头到冰柜)。生物银行软件(FreezerPro Brooks, Chelmsford, MA, USA)将用于记录以及样本和其他跟踪。样品将根据已验证的程序进行存取和提取,并根据试验方案进行分析。任何未使用的样品将在试验结束后保存至少5年。