学习设置{9}
德国耶拿大学医院,神经内科门诊部/物理治疗研究所
德国大学医院,神经退行性疾病/肌张力障碍中心门诊,Tübingen
另外两个研究中心正在计划中。所有参与者获得相同的研究程序和设备,包括相应的测量培训。
资格标准{10}
谁会接受知情同意?{26}
各自研究中心的医学研究主任(首席研究员)将接受知情同意。
关于收集和使用参与者数据和生物标本的额外同意条款
不适用。
干预措施
选择比较国的解释
从目前可用的数据可以得出结论,多模式附加PT,侧重于积极锻炼,在疼痛、CD的严重程度和日常生活活动方面,与单一的BoNT疗法相比具有优势。参与者将随机分配到多模式PT + BoNT干预组或BoNT +拔火罐组。拔火罐疗法被选为比较者(对照组),与一项技术进行比较,该技术包括治疗师在不直接通过颈肌张力障碍受影响的肌肉上被动应用。此外,拔火罐疗法可减轻慢性颈部疼痛,这在乳糜泻患者中很常见[20.].然而,没有证据表明拔火罐治疗会影响ZD患者的颈椎活动能力、疾病严重程度或生活质量。由于PT干预的性质,治疗师和参与者不能对治疗分配盲目。然而,评估TWSTRS的评分者对于患者的治疗组将是盲的。
干预描述{11a}
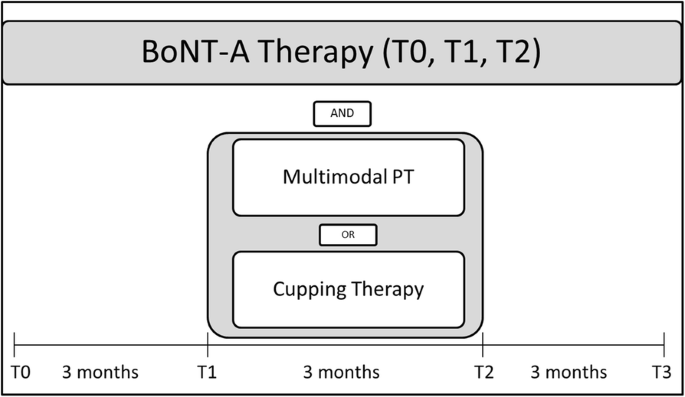
每位参与者的研究时间为9个月,分为三个阶段,每个阶段3个月。在第一阶段,两组患者均接受常规BoNT治疗。在第二阶段,各自的干预开始。在此期间,干预臂执行附加的多模式PT计划,其中包括24次PT会话,而控制臂则接受24次附加的非特定拔罐治疗。第三个阶段包括3个月的双臂BoNT治疗作为随访期。根据BoNT注射间隔,每3个月对参与者进行一次评估。这意味着有四个评估时间点:第一期开始时,干预期开始时,干预期结束时,分别是第三期开始时和第三期结束时。
患者可以选择自己的物理治疗师。此外,每个物理治疗师都会收到一份治疗建议(表1).他们没有义务使用每一个提到的技术,但他们应该分配他们的治疗不同的建议与评估。
A组:干预:物理治疗- 24个治疗单位,每周2次,持续30分钟B组:对照组:拔罐治疗(干,CT)
CT的目标是充血和代谢激活结缔组织的自我调节。此外,缓解疼痛和放松是CT的进一步目标。最长持续时间约为15分钟,或在血肿明显形成的情况下或在眼镜掉落的情况下。治疗应应用于病人的肩带,特别是肩袖(冈下肌和冈上肌)、菱形体(大菱形肌和小菱形肌)和胸部肌肉(胸大肌).
停止或修改已分配干预措施的标准{11b}
DysPT-Multi研究是一项介入性研究,但不是人类临床药物试验。与研究治疗相关的风险很少,但患者接受BoNT-A(不是一种研究药物,而是一种介入性药物)作为标准。这种伴随的药物有已知的风险。由于该研究是根据《赫尔辛基宣言》并遵循ICH-GCP指南进行的,因此已经实施了关于研究治疗和BoNT-A给药的安全管理。为此,在临床研究过程中观察到的不良事件将由研究中心记录和评估,并由研究主任定期重新评估与研究疗法或BoNT-A给药的因果关系。在个体化物理治疗的背景下,可以假设患者的安全水平很高。BoNT-A标准治疗更有可能发生不良事件。
提高干预依从性的策略{11c}
物理治疗实践将为研究中心提供咨询和随访的联系信息。
试验期间允许或禁止的相关伴随护理
将询问并记录伴随的治疗或药物。在意向-治疗分析中,将研究期间用药的变化记录为试验计划偏离/查询。尽管如此,患者将坚持在研究小组直到研究结束。
审判后护理的规定{30}
不适用。
结果{12}
主要终点:
二次端点:
参与者时间线{13}
参与者时间轴见表2和无花果。1
.
样本容量{14}
在先导试验中[19],经PT + BoNT干预后,总TWSTRS平均降低8.7点。BoNT和PT + BoNT干预的标准差分别为7.4和5.4点。若两组之间的差异不少于3点,且幂值为90%,则每组需分析100例患者。假设退出率为10%,总共224例患者(每组112例)被随机纳入试验。
招聘{15}
各研究中心的医学首席研究员在神经内科门诊招募患者。
干预措施的分配:分配
序列生成{16a}
计算机生成随机数,由软件“随机工具”生成
耶拿大学医院临床研究中心提供的基于互联网的随机化工具将执行随机化。这将在患者签署患者同意书后进行,符合所有纳入标准且没有排除标准,因此已纳入研究。
隐藏机制{16b}
小组分配由各自研究中心的医学研究主任分配。患者获得相应的治疗信息,并将其交给治疗师。
实现c {16}
由各自研究中心的医学研究主任负责
干预的分配:盲法
谁将被蒙蔽双眼
如有需要,可进行开盲操作。
不适用。
数据收集和管理
评估和收集成果的计划
评估员在招聘开始前接受过特别培训,并且/或已经对不同的测量方法有经验。
本研究的主要终点是多伦多西部痉挛性斜颈评分量表(TWSTRS)的总分。TWSTRS疾病特异性评分系统被开发用于描述乳糜泻的严重程度[21].该测量工具被广泛使用,并被明确推荐用于比较研究或进行元分析[2,12].可以确认评分的效度和信度[21].本研究采用盲法检查收集TWSTRS。总分范围为0-85分,得分越高,表达或损伤越严重[22].
次要终点为TWSTRS分量表(严重程度、日常生活限制和疼痛)、使用惯性传感器进行三维运动分析评估的颈椎活动度(ROM)(公司:Velamed)、SF-36问卷[23]以评估一般的健康认知,以及CDQ-24问卷[24来评估特定疾病的生活质量。此外,计划按年龄、严重程度、疾病持续时间和BoNT治疗持续时间进行亚组分析。
如有必要,将针对TWSRTS的各个子量表调查附加多模态PT的影响,以呈现更具体的影响。
颈肌张力障碍的临床相关性是颈椎错位或错位,包括邻近肌肉和关节。因此,颈椎的静力学和活动能力是评估干预效果的重要参数。为了能够获得尽可能客观的数据,基于仪器的三维测量系统(公司:Velamed)确定该终点的颈椎运动程度。该系统基于超声波测量信号,可以准确地确定所有三个运动平面的运动。有效性和重现性已成功验证[25].另一种具有类似技术基础和精确运动分析的测量仪器已经可以在乳糜泻患者中进行评估,并被推荐用于诊断和进展记录[26].此外,一个类似于三维运动测量的测量系统(Zebris公司)在试点研究中成功用于运动分析[19].然而,用惯性传感器测量更精确。
SF-36为研究提供了一个跨疾病评分系统来评估生活质量。有效性和可重复性已经过测试[23].
为了评估疾病特异性健康感知,使用CDQ-24问卷。本问卷旨在评估CD和/或眼睑痉挛患者的生活质量。原始问卷有德文版本。效度和信度均可用[24].
计划促进参与者保留和完成随访{18b}
患者由神经内科相应门诊定期安排,因此坚持研究方案时间线。
数据管理{19}.
数据收集是为了科学目的。数据是在参与研究的中心生成的。临床研究所需的所有数据都由研究中心的相应工作人员在基于计算机的在线数据输入系统中输入,并立即传输到耶拿临床研究中心(CCS)的服务器。
数据输入通过耶拿大学医院CCS服务器上的web应用程序执行,使用研究管理软件“OpenClinica®”。该软件满足法规要求(GCP, 21CFRPart11)。数据通过web浏览器的输入掩码加密数据连接(HTTPS)收集。为了确保数据分析的匿名性,每个患者都被分配了一个唯一的患者识别号。
研究管理软件“OpenClinica®”也用于数据管理。数据的可信度是通过范围、有效性和一致性检查来检查的。不可信或缺失的数据在研究中心进行查询。对数据的每一个更改,例如,由于回答的查询的合并,都通过自动更改跟踪(审计跟踪)记录在数据库中。使用分层的、基于角色的访问概念使得不可能对数据进行未经授权的访问。
作为一个文档中心,耶拿大学医院的CCS还负责数据存储。电子数据的备份定期进行。数据存储设施位于一个上锁的中心房间,只有系统管理员可以访问。
保密{27}
保证了评估范围内数据的匿名性。患者和患者ID之间的分配是通过患者识别列表在各自的研究中心进行的,而不是存储在数据库中。每天对所有数据进行完全备份。患者识别列表存储在相应的研究中心文件夹(研究者站点文件,ISF)中。
本试验/未来使用{33}的生物样本收集、实验室评估和存储计划用于遗传或分子分析
不适用。
统计方法
主要和次要结果的统计方法{20a}
主要终点(TWSTRS总分)采用线性混合模型进行评估。在模型中,干预(特定物理治疗或控制治疗)被视为固定因素,研究中心被视为随机因素。此外,通过将该变量作为协变量纳入模型,对基线TWSTRS总分进行了调整。治疗差异验证性检验的显著性水平为5%。
每个次要终点将拟合线性混合模型。干预被建模为一个固定因素和中心作为一个随机因素和各自的基线变量包括作为一个协变量。所有次要终点将在5%显著性水平下进行探索性比较。
(Intention-to-treat-analysis)
对于所有终点,将提供组特有的描述性统计(均数±标准差)。
中期分析{21b}
这些都不是计划中的。
附加分析的方法(例如,亚组分析)
所有终点附加定义为亚组,并按年龄、CD严重程度和既往接受过PT进行分析。
处理协议不遵守的分析方法和处理缺失数据的统计方法{20c}
主要分析将是意向治疗,包括所有随机患者,无论是否遵守方案。在严重不遵守方案的情况下,将进行二次分析,以估计每个方案的干预效果。
提供完整协议、参与者级别数据和统计代码的计划{31c}
不适用。
监督和监测
协调中心和试验指导委员会的组成
必须确保每个负责病例报告表格(CRF)文件的人都能被识别出来。研究文件夹中有允许在CRF(签名/授权日志)中进行记录的人员的签名和缩写。
本概述还包括参与临床试验的其他人员的姓名、签名、缩写以及他们的职责和权限。一份有签名和缩写的人员名单被归档在研究文件夹中。
数据监测委员会的组成、作用和报告结构
根据良好临床实践指南(ICH GCP E6),为保证质量,在较小范围内建立监测。监测临床研究的目的是确保临床研究是按照批准的方案进行的,并且符合伦理法规和标准。研究主任委托CCS Jena完成这项任务。监测包括在招募开始前对研究团队进行培训和简介的中央启动/网络研讨会、定期现场访问以及正确关闭研究地点的最后访问。监测将根据CCS耶拿的标准操作程序进行。由研究主任发布的监测手册中详细描述了监测的范围、程序和内容,以及确保数据质量的程序和在违反规程时采取的必要措施。研究医师将允许监测人员直接访问与研究相关的原始数据和文件。监测人员必须对所有信息保密,并维护研究参与者的基本完整性和隐私权。
不良事件报告和危害{22}
在临床试验过程中,所有不良事件(AEs)和特殊情况报告均应记录在患者记录中,并及时记录在CRF中。伦理委员会在研究主任评估后,每年收到一次严重的不良事件名单。
审核试运行的频率和计划{23}
审核是对与临床研究相关的活动和文件进行的系统和独立的审查,以确定与研究相关的活动是否按照方案、标准操作程序和适用的法律/伦理要求进行。作为质量保证过程的一部分,研究主任可随时在参与机构进行独立审计。在这种情况下,研究人员或参与机构将允许审核员检查审计所需的所有文件。
与相关方(如试验参与者、伦理委员会)沟通重要议定书修正案的计划{25}
在临床试验开始前发表积极意见后,必须通知负责的伦理委员会,例如,研究方案(修订)内容的变化、患者信息和同意书、额外的研究中心以及研究医生的变化。
传播计划{31a}
目前正在努力在国际著名医学杂志上发表这项临床试验的结果。