学习设置{9}
这项多机构随机对照试验将在韩国广域城市的五家医院进行:(1)亚洲大学医院,(2)汉阳大学九里医院,(3)梨花女子大学首尔医院,(4)首尔国立大学盆唐医院,(5)韩国天主教大学仁川圣玛丽医院。所有五家医院都是区域转诊和教育机构,有530多张病床,可为住院和门诊病人提供服务。另外,首尔大学盆唐医院是公立医院,其他医院由私立学术财团运营。
资格标准{10}
符合条件的患者是>,18岁,根据医生决定需要置入PICC的住院患者。由于CLABSI的诊断需要至少48小时的居住时间,因此排除置管后2天内即将出院或转院的患者。此外,本研究将是务实的,参与者不会因持续的医疗状况而被排除在外,例如持续的感染、恶性肿瘤或免疫。数字1所示为本研究的CONSORT流程图。tpicc和cpicc将由一名介入放射科医生在本研究指定的每个机构进行。将在门诊接受治疗的参与者将不包括在内,因为可能会遗漏感染相关症状。
谁会接受知情同意?{26}
大多数情况下,从人保的请求到在所有五家医院实施,只需要一个工作日。每个机构的调查人员应在PICC放置前至少1天获得知情同意。对于有紧急医疗需要的患者(由转诊医生决定),应在手术后至少6小时内获得知情同意。在获得知情同意之前,调查人员将向参与者提供信息表和对研究的详细解释。
关于收集和使用参与者数据和生物标本的额外同意条款
不适用。
干预措施
选择比较国的解释
我们假设,与传统方法相比,使用皮下隧道进行PICC插入将降低CLABSI发生率。
干预描述{11a}
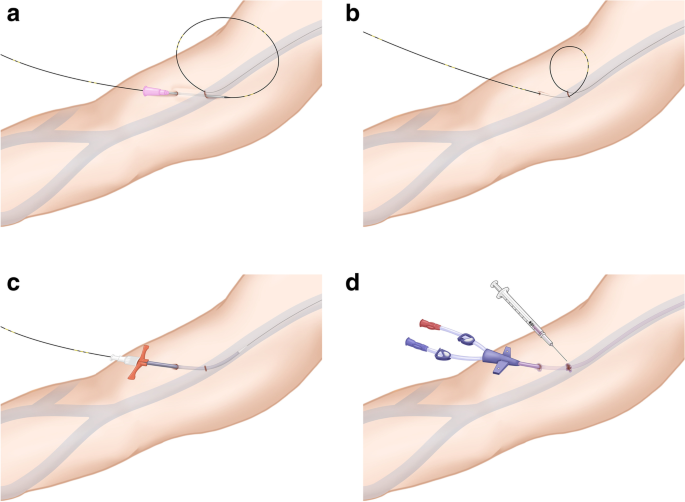
参与者将被分为两组。cPICC组在血管造影组超声和透视引导下,采用传统方法置入PICC。程序将在手卫生、最大无菌屏障和洗必泰的条件下执行。目标臂将用洗必泰和异丙醇的混合物消毒,并将无菌悬垂物从头到脚覆盖整个手术区域[14].将使用来自供应商的5-法国双腔PICC (UNIS;Genoss Co.,京畿道,韩国)。tPICC组将以同样的方式进行PICC放置,并附加皮下隧道。大多数商用picc不包含隧道或涤纶袖口。因此,在静脉穿刺后,将像往常一样放置镍钛诺导丝。我们将使用另一根18号针在初始静脉穿刺点远端2-3厘米处做一个隧道,导丝将逆行穿过针。在静脉穿刺部位的环分解后,将在导线上放置一个剥离的护套。在以通常的方式插入导管之前,导管将被修剪到静脉穿刺点和腔房连接处加上皮下隧道之间的距离。最初的静脉穿刺和出口部位的伤口将用少量的n-butyl-2-cyanoacrylate(无花果。2).
停止或修改已分配干预措施的标准{11b}
不愿意参加试验或在手术后48小时内意外丢失PICC的患者将被排除在研究之外。没有修改已分配干预的标准。
提高干预依从性的策略{11c}
本研究包括手术过程中的一次性干预,是一项实用主义研究。所有的手术都将由介入放射科医生进行。调查人员将通过标准手册和研讨会分享有关隧道方法的程序细节
试验期间允许或禁止的相关伴随护理
不适用。这是一项实用主义研究。插入PICC后,参与者将根据其病程进行治疗。在审判期间,不提供也不禁止相关的伴随护理。
审判后护理的规定{30}
皮下隧道是一种广泛使用的中心静脉导管放置手术,没有严重的并发症报道。然而,调查人员将努力减轻干预造成的损害。当无法从不可逆转的伤害中恢复时,本研究的保险计划将提供赔偿。患者不会因参与研究而获得补偿。
结果{12}
主要结果是PICC置入时皮下隧道对CLABSI发生率的影响。我们将使用国家医疗安全网络监测定义[15].CLABSI将被定义为实验室确认的血流感染,其中PICC存在超过48小时,必须满足以下两个标准:参与者通过培养或非培养的微生物学测试从一个或多个血液标本中鉴定出病原体,并且血液中鉴定出的生物体与其他来源的感染(例如粘膜屏障损伤)无关。一个委员会认证的感染疾病专家将在每个机构诊断CLABSI,独立于本盲法研究。
次要结果包括局部感染和出口部位出血的比率,皮下隧道的额外手术时间,以及技术成功率,定义为导管尖端成功放置到腔心房连接处的比率。局部感染定义为以下一种或多种症状:插入部位肿胀伴压痛、局部发热感或脓。当PICC因持续出血而无法固定时,将标记出口部位出血。轻微渗液导致换药不计入此结果。我们将把技术上的成功分为两类。如果穿刺目标静脉或将导管放置到腔房连接处失败,我们将其定义为“不可能PICC”。如果在目标静脉穿刺后出现皮下隧道失败,我们将其解释为“不可能的隧道”。
参与者时间线{13}
计算* * |
研究期间 |
招生 |
分配 |
Post-allocation |
清仓大拍卖 |
−1-3天 |
0 |
直到取出导管或出院 |
拔管或出院后 |
报名: |
资格的屏幕 |
X |
|
|
|
知情同意 |
X |
|
|
|
人口统计信息 |
X |
|
|
|
分配 |
|
X |
|
|
干预措施: |
传统的中国人民保险公司 |
|
|
X |
|
挖过的中国人民保险公司 |
|
|
X |
|
评估: |
人口统计资料 |
X |
|
|
|
实验室测试 |
X |
|
|
|
过程的细节 |
|
|
X |
|
Procedure-associated并发症 |
|
|
X |
|
延迟并发症 |
|
|
|
X |
样本容量{14}
根据此前有关中国人保的报道,感染率在0.6至7.4%之间[1,3.,4,5].在之前的回顾性研究中,tPICC的CLABSI率为2.6% [13].本试验假设相同的感染率计算样本量,以验证之前的回顾性研究结果。在本试验中,需要2 × 677名参与者来证明主要结局的感染率从6.2降低到2.6%,双侧α水平为0.05,统计功率为90%。本研究共纳入1694名参与者,退出率为20% (PASS,版本16,NCSS统计软件)。数据将根据他们最初分配的组在意向治疗的基础上进行分析。
招聘{15}
根据纳入和排除标准,所有要求PICC的住院患者均为本研究的潜在候选患者。独立于本研究的医生将与参与者讨论PICC的必要性。如果参与者同意置管,他们的医生将通过电子病历系统咨询介入放射学。调查人员(介入放射科医生或临床研究协调员)将审查参与者的医疗记录,介入放射科医生将访问他们的病房以获得知情同意。在获得知情同意时,每位候选人将进行尊重的讨论,以确保为患者做出谨慎的决定。通过非竞争性招募,五个研究所各招收339名患者。
干预措施的分配:分配
序列生成{16a}
随机化数字将由R程序(包' blockrand '中的blockrand函数)使用1:2到1:6的随机块生成。独立统计人员生成多个数据集,独立研究组织者(Medsoft, Hwasung京畿道,韩国)将在盲法的情况下将其中一个数据集应用于电子病例报告表格(e-CRF)。
隐藏机制{16b}
在手术前和无菌皮肤准备后,一名不参与试验的流动护士将访问安全的、有密码保护的、在线随机数据库。护士应告知调查人员受试者属于cPICC或tPICC组。
实现c {16}
一个独立的统计学家将创建计算机生成的块随机列表。然后,每个知情同意的符合条件的参与者将被送往血管造影套件,并在手术前由血管造影套件的独立循环护士随机分配到一组。
干预的分配:盲法
谁将被蒙蔽双眼
在这种类型的随机对照试验中,干预措施不能对干预者、参与者或护理提供者盲化,因此存在不可避免的偏倚风险。然而,由于以下原因,本研究具有单盲特征。参与者只能根据他们的伤疤推测他们的手术,但他们不能确定他们的小组,因为手术将在无菌窗帘下进行,以筛查患者的视觉确认。由于隧道是皮下的,很难判断是否做隧道,常规PICC也可以做多个皮肤切口。此外,干涉主义者不会确认他们的团体。至于护理提供者,主要是病房护士也可以假设该群体,但由于与参与者相同的原因不能确保分配。结果评估者对分配不知情。分配的e-CRF将不能被结果评估人员访问。在研究结束前,数据分析师将被盲。
如有需要,可进行开盲操作。
这项研究是无盲的。
数据收集和管理
评估和收集成果的计划
根据务实的研究,参与者将根据最初的治疗计划对他们的病情进行治疗。按照治疗计划进行每日体检和实验室检查。当参与者出现感染症状或体征时,将像往常一样进行血液培养和实验室检测。实验室检测包括白细胞分化计数、红细胞沉降率和c反应蛋白水平。
计划促进参与者保留和完成随访{18b}
本研究计划纳入住院患者,评估住院期间的不良事件(AEs)。我们没有提高留存率的计划。
数据管理{19}.
所有数据将被保存在医院外的独立在线服务器(Medsoft)中。调查人员将负责所有数据的录入和管理。至少两名调查人员将检查所有数据。
保密{27}
所有收集到的数据都将被编码为一个编码号码,在研究期间仅参考参与者的身份,以保持匿名。知情同意书将被锁在每个医院有密码锁的安全地方的一个上锁的柜子里。根据韩国《生命伦理安全法》的“登记令”,数据将在本次研究结束后保存3年。在此之后,所有数据都将被销毁,但在机构审查委员会(IRB)的许可下,数据存储扩展是可能的。
本试验/未来使用{33}的生物样本收集、实验室评估和存储计划用于遗传或分子分析
将视临床情况进行必要的实验室血液检测和培养
统计方法
主要和次要结果的统计方法{20a}
独立样本t-tests还是Mann-WhitneyU将使用检验(连续变量)和卡方检验或Fisher精确检验(分类变量)来比较两个研究组。数据将采用聚类分析,包括医院级别、ICU与普通病房。感染(CLABSI)率将以每1000导管驻留日的发生率报告[16].两组的比率和95%置信区间p-value将通过精确的速率比测试计算,假设泊松计数。Cox比例风险回归将用于估计“到感染时间”的调整风险比和95%置信区间(ci)。“每一种并发症的风险比均为95% ci。一个p-value小于0.05将被认为是显著的。
附加分析方法(如亚组分析)
亚组将根据其伴随疾病进行划分,包括糖尿病、恶性肿瘤(或恶性血液病)、免疫功能不全(人体免疫缺陷病毒感染或器官移植)、终末期肾病或以上疾病的合并症。
处理协议不遵守的分析方法和处理缺失数据的统计方法{20c}
不遵守协议后产生的数据将不包括在研究中,并将被披露。将努力将丢失的数据减少到最低限度。我们将处理丢失的数据与多个imputations (MICE Package, R ver。4.0.3, R统计计算基金会,维也纳,奥地利)。缺失的值将根据指引进行适当处理[17]
提供完整协议、参与者级数据和统计代码的计划{31c}
整个协议将在注册网站上发布。
监督和监测
协调中心和审判指导委员会的组成
五名作者(每个研究所一名)对科学有效性、研究质量、研究进行、程序、ae后的患者管理以及最终研究结果和报告的质量全权负责。所有五位作者都通过定期会议分享信息,并在出现问题时讨论研究和适当的管理。
数据监测委员会的组成、作用和报告结构
每个监测成员将在每个研究所进行数据监测。在监测过程中,数据监测委员会(DMC)将检查受试者的源文件是否合适,确认同意获取过程和存储是否合适,审查总体试验表现,进行e-CRF审查,审查研究人员的活页夹,收集受试者的任何ae,并进行跟踪。此外,委员会还计划通过安全评价验证和资料收集等方式进行监督。
随访期间检查任何与导管相关的不良事件,并在e-CRF中记录。如果出现超过II级的AE,将在24小时内报告给首席研究员(DJ Shim)。每个DMC成员将判断该AE是否与手术有关,任何相关的AE将立即报告给IRB和首席研究员。每位研究员应在15天内向IRB报告任何严重AE(≥III级)和任何其他意外问题。
三名独立成员将被任命为数据和安全监测委员会(DSMB;Seungjae Lee[韩国首尔国立大学融合科学与技术研究生院应用生物工程系],Young Seo Cho[韩国京畿道古里市汉阳大学九里医院放射科],Minuk Kim[首尔市政府-首尔国立大学博拉美医学中心放射科])。
不良事件报告和危害{22}
不良事件将根据不良事件通用术语标准(CTCAE)指南进行分类[18].如果一个地点发生三个以上的轻微不良事件(< III级),该地点的调查人员将向DSMB报告不良事件。如果发生一次严重的AE (CTCAE III、IV或V),将召开DSMB会议进行安全性评估。此外,每个研究机构的研究团队将对每个病例进行日常检查,并与其他研究团队进行沟通。
审核试运行的频率和计划{23}
在每收集200例新病例之前,由独立监测员对患者进行监测,如果病例没有达到200例,则每三个月进行一次监测。各机关检查中心委派视察员对审判活动和文件进行系统检查。患者和数据评估将独立于每个机构的研究人员或试验发起人进行。
中期分析{21b}
不进行中期分析。
向相关方(如试验参与者、伦理委员会)传达重大方案修订的计划{25}
本试验方案的任何变化将报告给每个研究所和试验登记处的IRB。
传播计划{31a}
这项研究的结果将发表在同行评议的医学杂志上。