研究设计
这是一项单中心、前瞻性、优势、双盲、随机、对照的临床试验。该研究已获得首尔大学盆唐医院机构审查委员会(B-2007-625-006)的批准。在患者首次到门诊进行资格筛选时,首席研究员将获得参与的书面知情同意。术后实验组给予5%利多卡因贴片(利多顶卡他匹;SK化学有限公司,Seongnam, Korea)和对照组将接受为本研究专门制作的安慰剂贴片。比较器是一个制作精良的安慰剂贴片,用于评价5%利多卡因贴片的疗效和安全性。研究设计概述如图所示。1.
假设
本研究的主要目的是评估5%利多卡因贴片对在日间手术单元接受单侧腹股沟疝修补术的患者术后急性疼痛的疗效。本前瞻性、优势、双盲、随机对照临床试验是基于以下假设设计的:应用利多卡因贴片的患者在单侧腹股沟疝修补术后出院时的VAS评分低于应用安慰剂贴片的患者。
纳入和排除标准
纳入标准为(a)年龄在19 - 80岁之间,(b)美国麻醉医师协会风险分类评分为I(健康)或II(轻微全身疾病),(c)单侧腹股沟疝择期开放手术,(d)手术当天入院和出院。
排除标准为:(a)肥胖(体重指数> 30 kg/m2), (b)肾功能不全(血清肌酐水平≥1.4 mg/dL), (c)肝功能不全(血清天冬氨酸转移酶水平≥120 IU/L或血清丙氨酸转氨酶水平≥120 IU/L), (d)已知对酰胺类局麻药过敏,(e)使用I类抗心律失常药物,如托卡因和美西汀,(f)拒绝参与。
本研究的主要研究人员不会基于种族或社会经济地位而排除可能参与本研究的患者。将尽一切努力确保尽可能多符合纳入标准的患者被纳入。患者将被告知这项研究的目的,以便他们能够代表接受全身麻醉的整个患者群体。
样本量计算
主要结局(出院时的VAS评分)的样本量是基于之前对腹疝患者的研究确定的,该研究比较了对照组(4.8±1.4)与利多卡因贴片组(3.1±1.6)的VAS评分,观察到差异为1.7 [9].对于I型误差(α)为5%,幂(1-β)为0.8的单侧分析,每组所需的参与者人数为14。预计退出率为10%,每组所需的参与者人数为16人,因此总样本量为32人。
随机化
我们将以1:1的比例将参与者随机分为利多卡因贴片组或安慰剂贴片组。我们将使用随机分配软件(伊斯法罕医学科学大学,伊斯法罕,伊朗)实现块随机化。来自麻醉科的研究护士(不参与研究)将生成随机分配序列并分发分配的贴片。这些贴片将直接交给麻醉师和外科医生,在手术结束时负责使用。评估患者临床参数的参与者和研究人员(麻醉师和外科医生)将对分组分配不知情。
过程
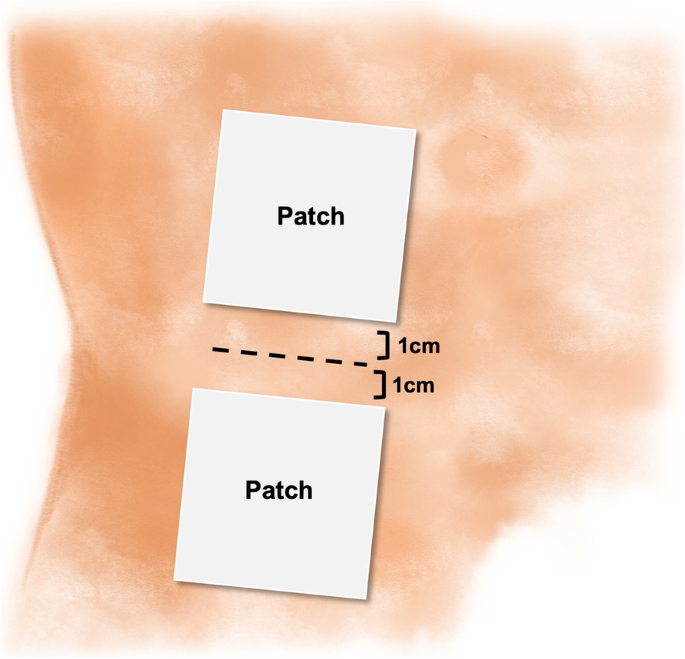
所有参与者将在全身麻醉下进行单侧腹股沟疝修补术。作为预处理,每位患者将在到达手术室时注射0.03 mg/kg咪达唑仑。麻醉师将使用常规方法吸入麻醉药和阿片类药物诱导和维持全身麻醉。普通外科医生将沿着皮肤褶皱线做一个大约3 - 4cm的横向切口,并进行常规的利希滕斯坦无张力补片腹股沟疝修补术。皮下间断缝合封闭皮肤,皮肤粘结(7 mm × 60 mm;将应用Leukosan SkinLink, BSN medical, Hamburg, Germany)。无菌敷料覆盖手术伤口后,根据随机分配顺序在手术伤口附近涂抹利多卡因或安慰剂贴片。每个患者将接受两个贴片,分别放置在手术伤口上方和下方1cm处(图2)。2).
从日间外科出院前,我们将允许参与者在全麻恢复期间使用额外的止痛药,如阿片类药物或非甾体抗炎药。芬太尼(50 μg;哈娜柠檬酸芬太尼,哈娜制药。Co., Ltd,首尔,韩国)或酮咯酸(30毫克;Trolac, Whan In Pharm。公司,有限公司,首尔,韩国)将被规定。芬太尼将最多开三次,当患者经历疼痛时,VAS评分为> - 5。如果患者在芬太尼给药后出现任何不良反应,将开酮乐酸。口服药物如曲马多/对乙酰氨基酚(37mg/325 mg;Rapicet, Chong Kun Dang Pharm。 Co., Seoul, Korea) will be prescribed to each patient at the time of discharge for pain management. However, additional pain medication or interventions outside of the protocol during the study period, which is from the surgery to 1 week after surgery, are prohibited.
本研究方案包括停止干预的标准。如果参与者撤回同意,随机分配后决定接受单侧腹股沟疝修补术以外的额外手术,或局麻药有任何不良反应,则终止研究。
结果
主要结果是出院时使用VAS测量疼痛强度,大约在手术后2或3小时。我们将在三种情况下评估每位患者的VAS评分:休息时、咳嗽时和移动时。次要结果是术后24小时和1周的疼痛强度。当贴片的镇痛效果消失后的第一天,当患者到诊所进行伤口敷料时,我们将评估每位患者的VAS评分。术后1周随访时,评估患者VAS评分、术后并发症(如恶心、呕吐、去饱和)发生率、出院后口服联合镇痛药总量。为了了解与全麻和利多卡因贴片的相关性,我们将额外分析术中阿片类药物的使用量、恢复时间和术后30分钟的疼痛强度作为次要结果的一部分。参与者的人口统计学特征,如年龄、性别、体重和身高,也将被记录。
学习记忆策略
所有参与者将收到一条短信,通知他们下一次门诊的日期、时间和地点,直到研究结束。如果没有出席,我们将亲自打电话给与会者以鼓励出席。
数据分析
所有统计分析都将使用Windows社会科学25.0版统计包进行(IBM,阿蒙克,纽约州)。将使用描述性统计分析参与者的人口统计学特征。在验证正态性后,采用学生t检验或曼-惠特尼检验U测试将用于分析数值数据。对于分类数据,我们将使用卡方检验或费雪精确检验。所有p值小于0.05的结果都被认为是显著的。
数据监控
首席研究员将在必要时,向参与者、首尔大学盆唐医院制度审查委员会、食品医药品安全处、审查委员会报告意外问题或不符合协议的情况。如果药物不良反应导致死亡或危及生命,应在7天内提交初次报告。如果药物不良反应不是致命的,应在15天内提交初步报告。轻微不符合规定的情况应每年逐案报告。
伦理与传播
为研究收集的信息将存储在实验室的一个锁定文件中,只有授权的研究人员才能访问研究文件。不必要的个人资料将被删除,患者姓名、居民身份证号码、病历号码等信息不应被记录。与个人信息相关联的识别码将单独管理。参与者的记录将被保密,不会被转移到其他地方,如有需要,参与者的记录可能会被发送给授权人士以监督本次研究。
我们将通过社交媒体向公众传播我们的研究方法和结果,在相应感兴趣领域的国内和国际会议上发表演讲,并向适当的科学期刊提交一篇描述我们发现的论文。